
 ��
�� +2NaOH$��_{��}^{H_{2}O}$
+2NaOH$��_{��}^{H_{2}O}$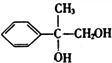 +2NaBr
+2NaBr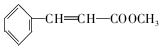 ��Ϊͬ���칹��
��Ϊͬ���칹��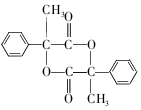 �ϳ�·������ͼʾ�����£�CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH$��_{Ũ���ᣬ��}^{CH_{3}COOH}$CH3COOCH2CH3��
�ϳ�·������ͼʾ�����£�CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH$��_{Ũ���ᣬ��}^{CH_{3}COOH}$CH3COOCH2CH3��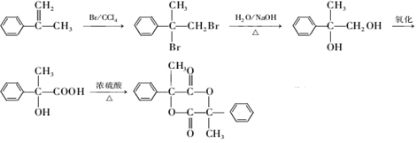 ��
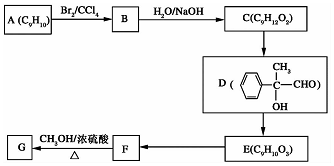
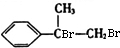
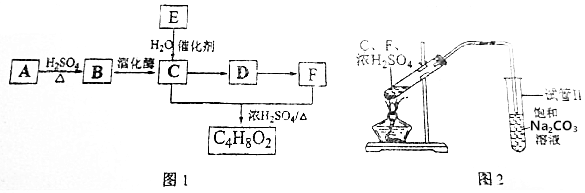
�� ���� A�ķ���ʽΪC9H10�������Ͷ�Ϊ5�����D�Ľṹ��֪AΪ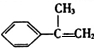 ��A���巢���ӳɷ�Ӧ����BΪ
��A���巢���ӳɷ�Ӧ����BΪ ��B����ˮ�ⷴӦ����CΪ
��B����ˮ�ⷴӦ����CΪ ��C��������������D������D��E�ķ���ʽ��֪��E��D��1��Oԭ�ӣ���֪D�е�ȩ��������Ϊ�Ȼ�������EΪ
��C��������������D������D��E�ķ���ʽ��֪��E��D��1��Oԭ�ӣ���֪D�е�ȩ��������Ϊ�Ȼ�������EΪ ��E��FΪ��ȥ��Ӧ��Eת���õ�F��F����״�����������Ӧ����G�������֪FΪ
��E��FΪ��ȥ��Ӧ��Eת���õ�F��F����״�����������Ӧ����G�������֪FΪ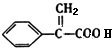 ��GΪ
��GΪ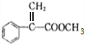 ���Դ˽��1������5����
���Դ˽��1������5����
��6����AΪԭ�ϣ��ϳ� ��A�ӳɵõ���±������ˮ�����ɶ�Ԫ��������������
��A�ӳɵõ���±������ˮ�����ɶ�Ԫ�������������� �������������Ӧ��
�������������Ӧ��
��� �⣺��1��������GΪ ����������̼̼˫����������C-D�ķ�Ӧ������������Ӧ��
����������̼̼˫����������C-D�ķ�Ӧ������������Ӧ��
�ʴ�Ϊ��̼̼˫����������������Ӧ��
��2��E�Ľṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��3��B��C�Ļ�ѧ��Ӧ����ʽΪ +2NaOH$��_{��}^{H_{2}O}$
+2NaOH$��_{��}^{H_{2}O}$ +2NaBr��
+2NaBr��
�ʴ�Ϊ�� +2NaOH$��_{��}^{H_{2}O}$
+2NaOH$��_{��}^{H_{2}O}$ +2NaBr��
+2NaBr��
��4��A�����з�������ͬ���칹���к���������1������ʱ����-CH2CH=CH2��-CH=CHCH2��������2�֣���2������ʱ�������ϩ�������������ڡ��䡢�����֣���5�֣��ʴ�Ϊ��5��
��5��a��1molE�ֱ�������Na��NaOH��Ӧ�����������ʵ���֮��Ϊ2��1���ʴ���
b��E��Һ�岻��Ӧ���ʴ���
c��G��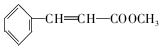 ����ʽ��ͬ���ṹ��ͬ����Ϊͬ���칹�壬����ȷ��
����ʽ��ͬ���ṹ��ͬ����Ϊͬ���칹�壬����ȷ��
d��F��̼̼˫��������ʹ��ˮ��ɫ������ȷ��
�ʴ�Ϊ��cd��
��6����AΪԭ�ϣ��ϳ� ��A�ӳɵõ���±������ˮ�����ɶ�Ԫ��������������
��A�ӳɵõ���±������ˮ�����ɶ�Ԫ�������������� �������������Ӧ���ϳ�����ͼΪ
�������������Ӧ���ϳ�����ͼΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л���ĺϳɣ�Ϊ��Ƶ���㣬���չ����ŵı仯��̼���仯���л���ӦΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע���л������ʵ�Ӧ�ã���Ŀ�Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl3��Һ�õ�FeCl3����--�������� | |
| B�� | ��ȥCu���л��е�CuO--����ϡ�����ܽ⡢���ˡ�ϴ�ӡ����� | |
| C�� | ����NaNO3��BaSO4�Ļ����--�ܽ⡢���� | |
| D�� | ��ȥNaOH��Һ�л��е�����Na2SO4--����BaCl2��Һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������μӵĻ�ѧ��Ӧ��������ѹǿ������С��Ӧ������������������ӻ���ӵİٷ������Ӷ�ʹ��Ӧ�������� | |
| B�� | ��ijһ�ﵽ��ѧƽ��״̬�ķ�Ӧ�����������ʹ��Ӧ���ʸı䣬ƽ��һ�����ƶ� | |
| C�� | �ڵ�⾫��ͭ�Ĺ����У����Һ��c��Cu2+����С | |
| D�� | 500�桢30 MPa�£���0.5 mol N2��g����1.5 mol H2��g�������ܱ������г�ַ�Ӧ����NH3��g������19.3 kJ�����Ȼ�ѧ����ʽΪN2��g��+3H2��g��?2NH3��g����H=-38.6 kJ•mol-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol•L-1 pH=7.82 �� NH4HCO3 ��Һ�У�c��HCO3-����c��NH4+����c��OH-����c��H+�� | |
| B�� | 0.1 mol•L-1 Na2S��Һ�У�c��OH-��=c��H+��+c��HS-��+2c��H2S�� | |
| C�� | Ũ�Ⱦ�Ϊ 0.1 mol•L-1��NH3•H2O ��Һ�� NH4Cl ��Һ�������ϣ�c��NH4+��+c��H+����c��NH3•H2O��+c��OH-�� | |
| D�� | 0.1 mol•L-1 Na2S ��Һ�� 0.1 mol•L-1 NaHS ��Һ�������ϣ�2c��Na+��-3c��S2-��=3c��HS-��+3c��H2S�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCN���ӵĽṹʽ��H-C��N | B�� | Se�ļ����Ų�ʽ��[Ar]4s24p4 | ||
| C�� | F-���ӵĽṹʾ��ͼ��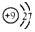 | D�� | ������̼�ĵ���ʽ 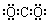 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | b��a��c | B�� | c��a��b | C�� | c��b��a | D�� | a��b��c |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ǵ�ȼ������2800 kJ•mol-1����$\frac{1}{2}$C6H12O6��s��+3O2��g���T3CO2��g��+3H2O��l����H=-1400 kJ•mol-1 | |
| B�� | ��֪101 kPaʱ��2C��s��+O2��g���T2CO��g����H=-221 kJ•mol-1����÷�Ӧ�ķ�Ӧ��Ϊ221 kJ•mol-1 | |
| C�� | ��֪ϡ��Һ�У�H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ•mol-1����ϡ������ϡ����������Һ��Ӧ����1 molˮʱ�ų�57.3 kJ������ | |
| D�� | ��֪HCl��NaOH��Ӧ���к��ȡ�H=-57.3 kJ•mol-1����98%��Ũ������ϡ����������Һ��Ӧ����1 molˮ���к���Ϊ-57.3 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.1g | B�� | 3.6g | C�� | 7.2g | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com