
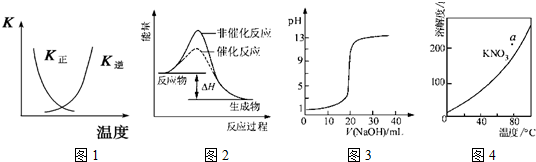
| A、图1表示该可逆反应平衡后,随温度升高,平衡会逆向移动 |
| B、图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| C、图3表示0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1醋酸溶液所得到的滴定曲线 |
| D、图4表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的过饱和溶液 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、此一元弱酸的电离常数(Ka)约为1.0×10-6 |
| B、此弱酸的浓度为1×10-4mol/L |
| C、此实验最好选用甲基红(变色范围在4.2~6.3)作指示剂 |
| D、此滴定反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某温度下,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )
某温度下,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )| A、加入Na2SO4可以使溶液由A点变到B点 |
| B、通过蒸发可以使溶液由D点变到C点 |
| C、D点无BaSO4沉淀生成 |
| D、A点对应的Ksp等于c点对应的Ksp |
查看答案和解析>>
科目:高中化学 来源: 题型:
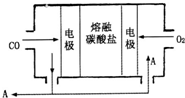 钠及其化合物具有广泛的用途.
钠及其化合物具有广泛的用途.| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


 是没食子酸的球棍模型,请结合有机结构特征,写出没食子酸的结构简式
是没食子酸的球棍模型,请结合有机结构特征,写出没食子酸的结构简式| NH2-NH2 |
| 水解 |
| 氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 甲、乙、丙、丁四种物质转化关系如右图.已知甲是一种导致钢铁生锈及许多还原性物质变质的单质,化合物乙、丙、丁均含有第三周期一种相同元素R.
甲、乙、丙、丁四种物质转化关系如右图.已知甲是一种导致钢铁生锈及许多还原性物质变质的单质,化合物乙、丙、丁均含有第三周期一种相同元素R.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com