
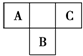
 A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.分析 A、B、C为短周期元素,由它们在周期表中的位置,可知A、C处于第二周期,B处于第三周期,令A原子核外电子为x,则B质子数为x+9,C核外电子数为x+2,则:x+x+2=x+9,解得x=7,故A为N元素、B为S元素、C为F元素,B原子核内质子数和中子数相等,均为16,然后结合元素的位置及周期律来解答.
解答 解:A、B、C为短周期元素,由它们在周期表中的位置,可知A、C处于第二周期,B处于第三周期,令A原子核外电子为x,则B质子数为x+9,C核外电子数为x+2,则:x+x+2=x+9,解得x=7,故A为N元素、B为S元素、C为F元素,
(1)由上述分析可知,A、B、C分别为N、S、F,故答案为:氮或N;硫或S;氟或F;
(2)C为F元素,原子核外有9个电子,各层电子数为2、7,原子的原子结构示意图为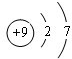 ,由原子结构可知元素的位置,则F位于第二周期ⅦA族,
,由原子结构可知元素的位置,则F位于第二周期ⅦA族,
故答案为:第二周期ⅦA族;
(3)非金属性F>S,C的氢化物与B的氢化物的稳定性强弱顺序为HF>H2S,故答案为:HF;H2S.
点评 本题考查元素的位置、结构与性质,为高频考点,把握元素的位置、原子结构及周期律推断元素为解答的关键,侧重分析与推断能力的考查,注意元素周期律及元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH=CH2 | B. | CH3(CH2)2CH(CH3)2 | C. | CH3CH2OH | D. | CH3C≡CH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2、O2、NO | B. | N2、O2、CO2 | C. | N2、NO | D. | N2、O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可以使溴水褪色 | |
| B. | 乙烯制备聚乙烯是物理变化 | |
| C. | 乙烷和乙烯互为同分异构体 | |
| D. | 乙烷可与氯气反应制取纯净的一氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 合理使用药物是保证身心健康、提高生活质量的有效手段.药物化学已经成为化学的一个重要领域.
合理使用药物是保证身心健康、提高生活质量的有效手段.药物化学已经成为化学的一个重要领域. 是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为
是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为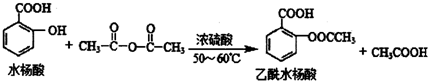
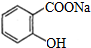 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用盐酸滴定氢氧化钠溶液时,滴定前,酸式滴定管内无气泡,滴定后也无气泡 | |
| B. | 用盐酸滴定氢氧化钠溶液时,用甲基橙作指示剂,接近滴定终点,溶液由黄色转变为橙色,但不足半分钟又转为黄色,继续滴加盐酸,溶液颜色又转变为橙色,持续半分钟后颜色不变 | |
| C. | 某学生要配制0.1 mol•L-1的稀硫酸100 mL,当加蒸馏水到离容量瓶刻度线1~2 cm处时,改用胶头滴管滴加,结果不慎使液面稍稍超过刻度线一点,将多余部分吸出,使凹液面最低点与刻度线相切 | |
| D. | 物质的量浓度为0.05 mol•L-1的NaOH标准溶液因与空气接触吸收了少量CO2,用此标准液滴定未知物质的量浓度的HCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属元素和非金属组成的化合物中的化学键一定是离子键 | |
| B. | 根据电离方程式HCl═H++Cl-,判断HCl分子里存在离子键 | |
| C. | 在水中分子间存在氢键作用,使水有较高的沸点 | |
| D. | 全部由非金属元素组成的化合物只能形成分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2+2H2O+4e-=4OH- | B. | Fe-3e-=Fe3+ | ||
| C. | Fe-2e-=Fe2+ | D. | 4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com