
| A、某酸式盐NaHY 的水溶液显碱性,则H2Y的电离力程式为H2Y=H++HY- |
| B、Na2CO3 溶液中存在:c(Na+)=2c(CO32-)+2 c(HCO3-)+2c(H2CO3 ) |
| C、在由水电离出的C(H+)=1×10-14mol?L-1的溶液中,可以大量存在Na+、K+、NO3-、HCO3- |
| D、在常温下,向10mLpH=12 的氢氧化钠溶液中加入pH=2 的HA 溶液至pH 刚好等于7,所得洛液体积v (总)≤20mL |


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:
| A、4.6mol/L |
| B、9.2mol/L |
| C、10.8mol/L |
| D、5.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
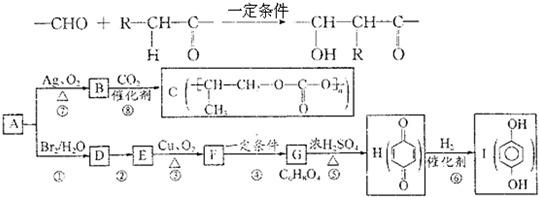
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5种 | B、6种 | C、8种 | D、9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
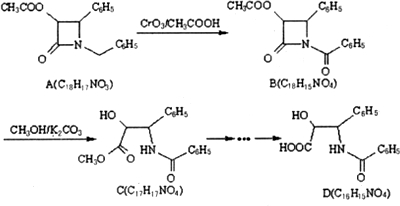
| K2CO3 |
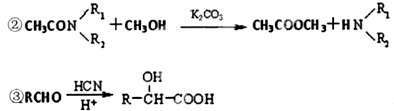
| PCl3 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
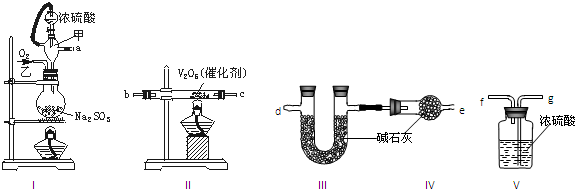
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢气在氯气中燃烧产生苍白色火焰 |
| B、金属钠长期暴露在空气中变成黄色 |
| C、钠在氯气中燃烧产生白烟 |
| D、过氧化钠投入水中生成的气体能使带火星的木条复燃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com