
【题目】下列装置或操作能达到实验目的的是( )

A. 用图1实验可证明非金属性Cl>C>Si
B. 用图2所示装置可除去NO2中的NO
C. 用图3装置制备Fe(OH)2并能较长时间观察其颜色
D. 图4实验装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性
科目:高中化学 来源: 题型:
【题目】NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020mol/LNaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是
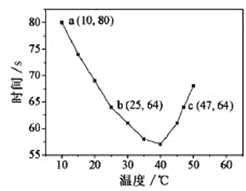
A. 40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
B. 图中b、c两点对应的NaHSO3反应速率相等
C. 图中a点对应的NaHSO3反应速率为5.0×10-5mol·L-1·s-1
D. 温度高于40℃时,淀粉不宜用作该实验的指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鉴别物质的方法错误的是( )
A. 用酚酞鉴别食盐水和稀醋酸
B. 用水鉴别生石灰和石灰石
C. 用燃着的木条鉴别空气和二氧化碳
D. 用氯化钡溶液鉴别稀盐酸和稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物。n是元素Z的单质。通常为黄绿色气体,q的水溶液具有漂白性。0.01mol/L r溶液的![]() 为2,p是甲烷。上述物质的转化关系如图所示。下列说法正确的是
为2,p是甲烷。上述物质的转化关系如图所示。下列说法正确的是
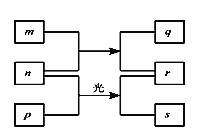
A.原子半径的大小W<X<Y
B.元素的非金属性Z>X>Y
C.![]() 的氢化物常温常压下为气态
的氢化物常温常压下为气态
D.![]() 的最高价氧化物对应的水化物为弱酸
的最高价氧化物对应的水化物为弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的氧化产物是甲,还原产物是乙,甲和乙都能与钠反应放出H2,甲和乙反应生成丙,甲和丙都能发生银镜反应。该有机物是
A. 甲醛 B. 乙醛 C. 甲酸 D. 甲醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会密切相关,下列有关说法中正确的是
A. “低碳生活”是指生活中尽量使用含碳量较低的物质
B. 燃煤中加入CaO后可减少酸雨的发生
C. 高纯铝被大量用于制造火箭、导弹和飞机的部件
D. 食品包装袋内的铁粉和生石灰的作用原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬是一种银白色的金属,化学性质稳定,用途广泛。 工业上以铬铁矿[主要成分是 Fe(CrO2)2]为原料冶炼铬及获得强氧化性 Na2Cr2O7,其工艺流程如下图所示:
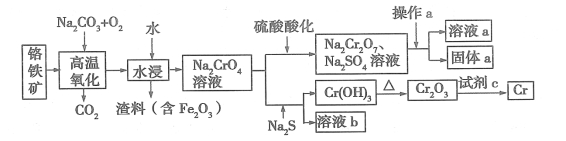
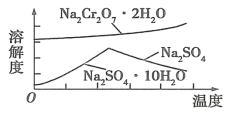 (1)Na2Cr2O7 中铬元素的化合价为 ,已知 Cr(OH)3 为两性氢氧化物,写出其电离方程式 。
(1)Na2Cr2O7 中铬元素的化合价为 ,已知 Cr(OH)3 为两性氢氧化物,写出其电离方程式 。
(2)写出利用铝热反应制取铬的化学方程式: ,试剂 c 通常还可以是 (至少写两种) 。
(3)酸化过程中,不选用盐酸的原因是 。
(4)固体 a 的主要成分是 Na2SO4·10H2O,根据图分析,操作a为 、 、过滤。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物有重要用途,如聚合硫酸铁![]() 是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:
是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:

请回答下列问题:
(1)若A为H2O(g),写出反应方程式:_________________________。
(2)若B为NaClO3与稀硫酸,写出其氧化Fe2+的离子方程式(还原产物为Cl-) 。
(3)若C为KNO3和KOH的混合物,写出其与Fe2O3加热共融制得高铁酸钾(K2FeO4)的化学方程式,并配平:
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com