

| ||
| 56L |
| 22.4L/mol |
| ||
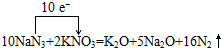 ,故答案为:
,故答案为: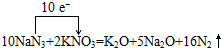 ;
;| 56L |
| 22.4L/mol |
| ||
| 10 |
| 16 |
| 2 |
| 16 |
| 10 |
| 16 |
| 2 |
| 16 |


科目:高中化学 来源: 题型:
| 物质 | 食醋 | 米酒 | 食盐水 | 肥皂水 |
| pH | 3 | 7.1 | 7 | 10 |
| A、食醋 | B、米酒 |
| C、食盐水 | D、肥皂水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、14 | B、38 | C、57 | D、无定值 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、98克H2SO4和H3PO4 含有的氧原子数均为4NA. |
| B、1L1mol?L-1 的硫酸与高氯酸(HClO4)溶液中含有的氧原子数均为4NA |
| C、33.6LNO2 溶解于足量的水中得到的硝酸溶液,溶液中NO3-数目为NA |
| D、32克铜发生氧化还原反应,一定失去NA 个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.5mol/L Na2S溶液中含Na+数目为5NA |
| B、1.00mol NaCl中,所有Na+的最外层电子总数为10NA |
| C、常温常压下,48gO2和O3混合气体中,含有氧原子数为3NA |
| D、标况下含NA个氮原子的N2和N2O的混合气体中,N2体积为5.6L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| B、在pH=8的NaB溶液中:c(Na+)-c(B-)=0.99×10-6 mol?L-1 |
| C、pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液中:c(NH4+)大小顺序①=②>③ |
| D、向10mL pH=12的NaOH溶液中滴加pH=2的HA溶液达中性:则混合液体积V总≥20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法中正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法中正确的是( )| A、该物质的摩尔质量为46 g?mol-1 |
| B、1 mol该物质含有9个共价键 |
| C、相同质量的该物质和S2N2所含原子个数之比为1:1 |
| D、该物质与S2N2互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com