
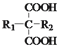 $\stackrel{△}{→}$
$\stackrel{△}{→}$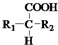 +CO2↑(R1和R2代表烷基)
+CO2↑(R1和R2代表烷基)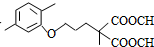 $\stackrel{△}{→}$
$\stackrel{△}{→}$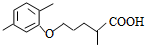 +CO2↑.
+CO2↑.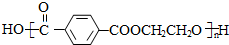 .
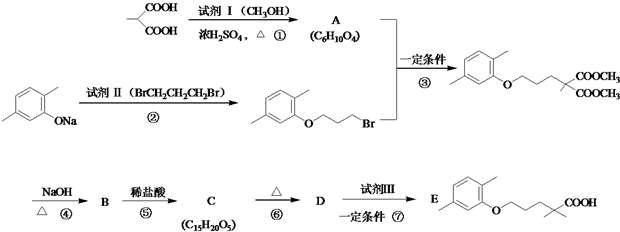
. 分析 (1)试剂I的结构简式为CH3OH,名称是甲醇;试剂Ⅱ的结构简式为BrCH2CH2CH2Br,含有的官能团为溴原子;对比 、
、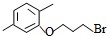 、BrCH2CH2CH2Br的结构可知,反应②属于取代反应;
、BrCH2CH2CH2Br的结构可知,反应②属于取代反应;
(2)反应①是CH3CH(COOH)2与CH3OH发生酯化反应生成CH3CH(COOCH3)2;
(3)反应④在碱性条件下发生酯的水解反应生成B,B酸化生成C,则C为 ,结合信息可知D
,结合信息可知D ;
;
(4)第⑦步反应中,试剂Ⅲ为单碘代烷烃,对比D、E的结构简式可知试剂Ⅲ为CH3I;
(5)C的分子式为C15H20O5,其同分异构体在酸性条件下水解,说明含有酯基,生成X、Y和CH3(CH2)4OH,生成物X含有羧基和苯环,且X和Y的核磁共振氢谱均只有两种类型的吸收峰,则X为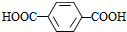 ,Y为HOCH2CH2OH.
,Y为HOCH2CH2OH.
解答 解:(1)试剂I的结构简式为CH3OH,名称是甲醇;试剂Ⅱ的结构简式为BrCH2CH2CH2Br,含有的官能团为溴原子;对比 、
、 、BrCH2CH2CH2Br的结构可知,反应②属于取代反应,
、BrCH2CH2CH2Br的结构可知,反应②属于取代反应,
故答案为:甲醇;溴原子;取代反应;
(2)反应①是CH3CH(COOH)2与CH3OH发生酯化反应生成CH3CH(COOCH3)2,反应方程式为:CH3CH(COOH)2+2CH3OH$?_{△}^{浓硫酸}$CH3CH(COOCH3)2+2H2O,
故答案为:CH3CH(COOH)2+2CH3OH$?_{△}^{浓硫酸}$CH3CH(COOCH3)2+2H2O;
(3)反应④在碱性条件下发生酯的水解反应生成B,B酸化生成C,则C为 ,结合信息可知D
,结合信息可知D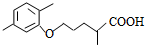 ,第⑥步反应的化学方程式是:
,第⑥步反应的化学方程式是:
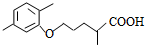 +CO2↑,
+CO2↑,
故答案为: $\stackrel{△}{→}$
$\stackrel{△}{→}$ +CO2↑;
+CO2↑;
(4)第⑦步反应中,试剂Ⅲ为单碘代烷烃,对比D、E的结构简式可知试剂Ⅲ为CH3I,
故答案为:CH3I;
(5)C的分子式为C15H20O5,其同分异构体在酸性条件下水解,说明含有酯基,生成X、Y和CH3(CH2)4OH,生成物X含有羧基和苯环,且X和Y的核磁共振氢谱均只有两种类型的吸收峰,则X为 ,Y为HOCH2CH2OH,X和Y发生缩聚反应所得缩聚物的结构简式是:
,Y为HOCH2CH2OH,X和Y发生缩聚反应所得缩聚物的结构简式是: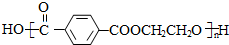 ,
,
故答案为: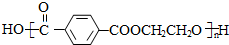 .
.
点评 本题考查有机合成和有机推断,涉及有机物的命名、官能团的识别、反应类型的判断、同分异构体、化学方程式的书写等,是对有机化学基础的综合考查,侧重考查学生分析推理能力.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
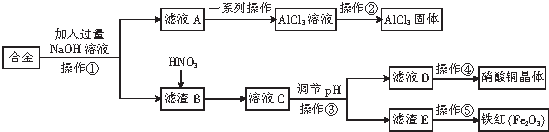
| A. | 滤液A中的溶质主要是NaAlO2和NaOH | |
| B. | 调pH时,可以加入CuO或Cu2(OH)2CO3 | |
| C. | 操作②是在蒸发皿中直接蒸干水分 | |
| D. | 该合金中含有的金属主要为铁、铜、铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 Na2O2可用作漂白剂和呼吸面具中的供氧剂.
Na2O2可用作漂白剂和呼吸面具中的供氧剂.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
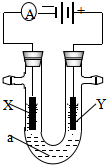 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
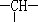 和一个-Cl,它的可能的结构有几种( )
和一个-Cl,它的可能的结构有几种( )| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3O4与足量稀 HNO3 反应:Fe3O4+8H+=2Fe3++Fe2++4H2O | |
| B. | 用小苏打治疗胃酸过多:NaHCO3+H+=Na++CO2↑+H2O | |
| C. | 双氧水中加入稀硫酸和 KI 溶液:H2O2+2H++2I-=I2+2H2O | |
| D. | 往碳酸氢钙溶液中滴入少量氢氧化钠溶液:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| C. | 向NaAlO2溶液中通人过量CO2制Al(OH)3:AlO2-+CO2+H2O═Al(OH)3↓+HCO3- | |
| D. | 向含2molAlCl3的溶液中加入1L 7mol/L的NaOH溶液:2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2是一种黄绿色、有刺激性气味、有毒的气体 | |
| B. | Cl2能使湿润的红色布条褪色 | |
| C. | Fe在Cl2中燃烧,生成的产物为FeCl2 | |
| D. | 实验室用加热二氧化锰和浓盐酸的方法制取Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com