
| A. | 13C和 14N 质子数相差 1,中子数也相差1 | |
| B. | 一种元素可以有多种核素,有几种核素就有几种原子 | |
| C. | 钴5627Co、5727Co、5827Co、5927Co等几种原子,他们是同素异形体,其物理性质几乎相同,化学性质不同 | |
| D. | 核聚变如21H+31H→42He+10 n,由于有新微粒生成,该变化是化学变化 |
分析 A.原子中质量数=质子数+中子数,元素符号左上角为质量数,左下角为质子数;
B.核素是指一定质子数,一定中子数的原子,同种元素质子数相同,中子数不同,质量数不同的原子为元素的同位素;
C.同素异形体是同种元素组成的不同单质;
D.化学变化的实质是旧键的断裂和新建的形成,化学变化是指有新物质生成的变化,是分子、原子层次上发生的变化;
解答 解:A.13C和 14N 质子数分别为6、7相差 1,13C中子数=13-6=7,14N 中子数=14-7=7,中子数相同,相差0,故A错误;
B.一种元素可以存在质子数相同,中子数不同,质量数不同的原子为元素的同位素,是不同的核素,所以一种元素可以有多种核素,有几种核素就有几种原子,故B正确;
C.钴5627Co、5727Co、5827Co、5927Co等几种原子是质子数相同中子数不同的同种元素的不同原子,是钴元素的同位素,不是单质不属于同素异形体,故C错误;
D.核聚变时原子种类发生变化,不存在旧键的断裂和新键的形成,不属于化学变化,也不属于物理变化,属于核变化,故D错误;
故选B.
点评 本题考查了原子结构、同位素、核素、同素异形体等知识点的理解应用,注意核聚变不是化学变化的理解判断,掌握基础是解题关键,题目难度中等.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢气与氯气反应生成2mol氯化氢气体,需要释放183kJ的热量 | |
| B. | 氢气与氯气反应生成2mol氯化氢气体,需要吸收183kJ的热量 | |
| C. | 氢气与氯气反应生成1mol氯化氢气体,需要吸收183kJ的热量 | |
| D. | 氢气与氯气反应生成1mol氯化氢气体,需要释放183kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.500 mol | B. | 1.00 mol | C. | 0.125mol | D. | 0.25 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ④③①②⑤ | C. | ④①②③⑤ | D. | ②③①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
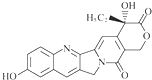
| A. | 可以与溴水反应 | |
| B. | 可以与FeCl3溶液发生显色反应 | |
| C. | 可以与浓HBr溶液反应 | |
| D. | 一定条件下,1 mol该物质最多可与1 mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
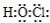 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向氯化铝溶液中滴加过量的氨水:4NH3•H2O+Al3+═AlO2-+4NH4++2H2O | |
| B. | NH4Al(SO4)2溶液中滴加少量NaOH溶液:Al3++NH4++4OH-=Al(OH)3↓+NH3•H2O | |
| C. | 向明矾溶液中加入过量的Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O | |
| D. | 向NaAlO2溶液中通入足量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
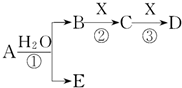 A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去):
A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com