
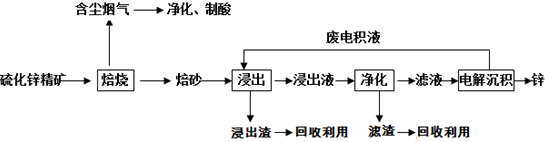
分析 硫化锌精矿的焙烧可生成ZnO、氧化铁等,含尘烟气含有含硫氧化物,可用于制备硫酸,浸出液加入硫酸可生成硫酸锌、硫酸铁,加入过量锌充分反应,可置换出铁,滤液中主要含有硫酸锌,经电解可得到锌和硫酸,电解液中含有硫酸,可循环利用,
(1)含锌矿的主要成分是ZnS,与空气中氧气发生氧化还原反应,判断焙砂的主要成分;
(2)焙烧生成的含硫氧化物可转换为硫酸;
(3)该含锌矿中还含有FeS等杂质,浸出操作后转化为亚铁离子,可加入锌粉出去亚铁离子,从而出去Fe;
(4)电解沉积过程中,是电解ZnSO4,阳极发生氧化反应,以此判断阳极产物;
(5)根据反应物和生成物写出化学方程式;
(6)依据硫化铜溶解度小于硫化锌,硫酸铜溶液遇到闪锌矿发生沉淀转化反应生成硫化铜;
(7)碳酸锌与碳在高温下反应生成锌和一氧化碳,结合氧化还原反应得失电子守恒配平方程式.
解答 解:硫化锌精矿的焙烧可生成ZnO、氧化铁等,含尘烟气含有含硫氧化物,可用于制备硫酸,浸出液加入硫酸可生成硫酸锌、硫酸铁,加入过量锌充分反应,可置换出铁,滤液中主要含有硫酸锌,经电解可得到锌和硫酸,电解液中含有硫酸,可循环利用,
(1)含锌矿的主要成分是ZnS,与空气中氧气发生氧化还原反应,则焙砂的主要成分为ZnO,故答案为:ZnO;
(2)焙烧生成的含硫氧化物可转换为硫酸,用于后续的浸出操作,故答案为:浸出;
(3)该含锌矿中还含有FeS等杂质,浸出操作后转化为亚铁离子,可加入锌粉出去亚铁离子,从而出去Fe,反应的离子方程式为Zn+Fe2+=Zn2++Fe,
故答案为:置换出Fe等;Zn+Fe2+=Zn2++Fe;
(4)电解沉积过程中,是电解ZnSO4,阳极发生氧化反应,产物为O2,故答案为:O2;
(5)“氧压酸浸”法顾名思义,可知反应物中含有H+和O2,可以获得非金属单质S,化学方程式为2ZnS+4H++O2=2Zn2++2S↓+2H2O,
故答案为:2ZnS+4H++O2=2Zn2++2S↓+2H2O;
(6)渗透到地下深层的硫酸铜溶液遇到闪锌矿,在一定条件下,溶解度小的矿物可以转化为溶解度更小的矿物(或在相同条件下,由于KSP(CuS)小于KSP(ZnS),故反应可以发生),硫化铜溶解性小于硫化锌,发生沉淀转化反应,反应的离子方程式:Cu2+(aq)+ZnS(s)=CuS(s)+Zn2+(aq);
故答案为:在一定条件下,溶解度小的矿物可以转化为溶解度更小的矿物(或在相同条件下,由于KSP(CuS)小于KSP(ZnS),故反应可以发生);
(7)碳酸锌与碳在高温下反应生成锌和一氧化碳,化学方程式为:ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑,故答案为:ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑.
点评 本题以流程题的形成考查物质的分离、提纯,为高考成常见题型,侧重于学生的分析能力、实验能力的考查,注意把握物质的性质以及实验的原理,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
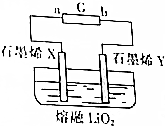 据英国《金融时报》网站最近报道,英国科学家研制出一种超容量的锂电池.其简易电池工作原理如图所示.X、Y是用石墨烯制成的渗透性极好的“蓬松”电极,其中石墨烯X极附着锂.该电池的工作原理是Li(s)+O2(g)$?_{充电}^{放电}$LiO2(s).下列说法不正确的是( )
据英国《金融时报》网站最近报道,英国科学家研制出一种超容量的锂电池.其简易电池工作原理如图所示.X、Y是用石墨烯制成的渗透性极好的“蓬松”电极,其中石墨烯X极附着锂.该电池的工作原理是Li(s)+O2(g)$?_{充电}^{放电}$LiO2(s).下列说法不正确的是( )| A. | 充电过程,电源G的b极为负极 | |
| B. | 放电过程,Y极发生还原反应 | |
| C. | 放电过程,X极的电极反应式为Li-e-+O2-═LiO2 | |
| D. | 充电过程,每转移2 mol电子,Y极放出44.8L(标准状况)O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n=5 | B. | n<5 | C. | n>5 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com