
| A. | 50% | B. | 40% | C. | 60% | D. | 30% |
分析 发生Fe+2Fe3+=3Fe2+,当溶液中的Fe3+与Fe2+的物质的量相等时,设均为3mol,结合反应计算.
解答 解:当溶液中的Fe3+与Fe2+的物质的量相等时,设均为3mol,
由Fe+2Fe3+=3Fe2+可知,参加反应的Fe3+为2mol,则原Fe3+总物质的量为3mol+2mol=5mol,
可知被还原的Fe3+的物质的量占到原Fe3+总物质的量的比例是$\frac{2mol}{5mol}$×100%=40%,
故选B.
点评 本题考查氧化还原反应的计算,为高考常见题型和高频考点,把握发生的反应为解答的关键,侧重分析与计算能力的考查,注意巧设数据简化计算,题目难度不大.


科目:高中化学 来源: 题型:选择题
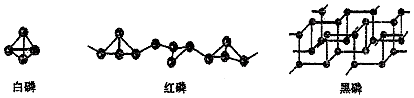
| A. | 属于同位素 | B. | 属于同分异构体 | ||
| C. | 都属于多原子分子 | D. | 黑磷在空气中不易燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜的熔点高于铝 | |
| B. | 向氢氧化镁悬浊液中加入浓的NH4Cl溶液,因发生化学反应而溶解 | |
| C. | 足量的Cu与含2molH2SO4的浓硫酸充分反应可生成NA个SO2分子 | |
| D. | 氢氧化铝溶于强碱溶液,说明铝具有一定的非金属性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为2NA | |
| B. | 在反应KClO3+6HCl═KCl+3Cl2+3H2O中,每生成3molCl2转移的电子数为6NA | |
| C. | 含4molSi-O键的二氧化硅晶体中,氧原子数为2NA | |
| D. | 某密闭容器中盛有0.2molSO2和0.1molO2,在一定条件下充分反应,生成SO3分子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn2+HCl=ZnCl2+H2↑ | |
| B. | Cu2(OH)2CO3+4HCl=2CuCl2+CO2↑+3H2O | |
| C. | HCl+AgNO3=AgCl↓+HNO3 | |
| D. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
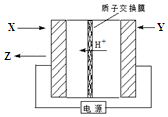 氨是生产氮肥、尿素等物质的重要原料.电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )
氨是生产氮肥、尿素等物质的重要原料.电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )| A. | 图中所示电极中,X端为负极,Y端为正极 | |
| B. | Y参与的电极反应为H2+2e-=2H+ | |
| C. | 反应过程中左边区域溶液pH逐渐升高 | |
| D. | 当有3gH+通过质子交换膜时,Z的体积为11.2L(标况) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com