
【题目】由乙醇制取环乙二酸乙二酯时,最简便的流程需要下列哪些反应,其正确的顺序是:①取代;②加成;③氧化;④还原;⑤消去;⑥酯化;⑦中和
A. ①②③⑤⑦ B. ⑤②①③⑥ C. ⑤②①④⑦ D. ①②⑤③⑥
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】在体积为2L的密闭容器中发生2SO2+O22SO3反应,现控制下列三种不同的条件:①在400℃时,10molSO2与5molO2反应;
②在400℃时,20molSO2与5molO2反应;
③在300℃时,10molSO2与5molO2反应;
(1)开始时,化学反应速率快慢顺序是;
(2)若10min内测得第①组的平均反应速率为:V(SO2)=0.4mol/(Lmin),则V(O2)= , 10min时,SO3浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化铝、磷化锌、磷化钙与水反应产生高毒的PH3气体(熔点为-132℃,还原性强、易自燃),可用于粮食熏蒸杀虫。卫生安全标准规定:当粮食中磷化物(以PH3计)的含量低于0.05mg·kg-1时算合格。可用以下方法测定粮食中残留的磷化物含量:
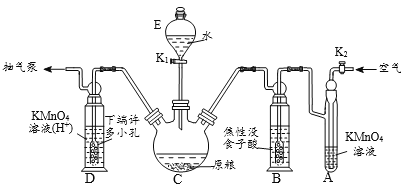
【操作流程】安装吸收装置→PH3的产生与吸收→转移KMnO4吸收溶液→亚硫酸钠标准溶液滴定。
【实验装置】C中盛100 g原粮,D中盛有 20.00 mL 1.12×10-4 mol L-1KMnO4溶(H2SO4酸化)。
请回答下列问题:
(1)仪器C的名称是_________;原粮最好先打成粉末,其原因是_____________。
(2)磷化钙与水反应有化学方程式为_____________________________________;检查整套装置气密性良好的方法是_______________________________________。
(3)A中盛装KMnO4溶液的作用是除去空气中的还原性气体;B中盛装焦性没食子酸的碱性溶液,其作用是吸收空气中的O2,防止___________;通入空气的作用是____________。
(4)D中PH3被氧化成磷酸,所发生反应的离子方程式为_________________________。
(5)把D中吸收液转移至容量瓶中,加水稀释至250mL,取25.00mL于锥形瓶中,用5.0×10-5mol L-1的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗标Na2SO3准溶液11.00mL,则该原粮中磷化物(以PH3计)的含量为______mg kg-1,该原粮质量________(填“合格”或“不合格”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的说法正确的是( )
A. 用 Ba(OH)2 处理含 Cu2+的废水,可消除水中重金属离子的污染
B. 某由 C、H、O 三种元素组成的有机物球棍模型如图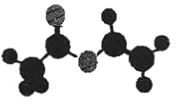 ,该化合物的链状同分异构体中(不考虑立体异构),能与 NaHCO3反应放出 CO2的只有 3 种
,该化合物的链状同分异构体中(不考虑立体异构),能与 NaHCO3反应放出 CO2的只有 3 种
C. 隔夜蔬菜中的部分硝酸盐被氧化为有毒的亚硝酸盐
D. 向铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色褪去,该过程中发生的反应为 2Al+3Ag2S=6Ag+Al2S3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g)△H=a kJ/mol 在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化数据如下表:下列说法不正确的是( )
温度 | 时间/min | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
A.10 min内,T1时CH4的化学反应速率比T2时小
B.温度:T1<T2
C.a<0
D.平衡常数:K(T1)<K(T2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pKa=lgKa,25℃时,H2A 的 pKa1=1.85,pKa2=7.19。常温下,用 0.1 mol/LNaOH 溶液滴定 20 mL 0.1 mol/LH2A 溶液的滴定曲线如图所示。下列说法正确的是( )
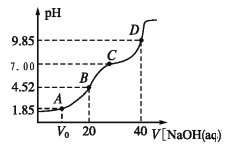
A. A 点所得溶液中:V0<10 mL
B. B 点所得溶液中:c(H2A)+c(H+)=c(HA-)+c(OH-)
C. C 点所得溶液中:c(A2-)= c(Na+)—c(HA-)—c(H2A)
D. D 点所得溶液中 A2-水解平衡常数 Kh1=107.19
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧、硫位于元素周期表的 VIA 族,其化合物在化工生产中有广泛应用。
(1)CuSO4可由 Cu+H2SO4+H2O2=CuSO4+2H2O 反应制得,该反应应要控制在 40—50℃,原因是________________________________________________。
(2)蛋白质中也含有硫元素,为了测定硫元素质量分数,取蛋白质样品充分燃烧,先用足量碘水吸收二氧化硫,再取吸收液,以淀粉为指示剂,用硫代硫酸钠溶液滴定过量的碘。已知:2S2O32-+I2=S4O62-+2I-
① 滴定终点的现象为:________________________________________。
② 取蛋白质样品 mg 进行测定,采用 C1mol/L 的碘水 V1mL 进行吸收,滴定过量的碘时消耗 C2mol/L 硫代硫酸钠溶液 V2mL。该蛋白质中的硫元素的质量分数为______________。
③ 若燃烧时过量氧气进入吸收液中,可能会导致该蛋白质中的硫元素的质量分数测定值___(填“偏大”或“偏小”或“无影响”)。
(3)苯硫酚(C6H5SH)是一种用途广泛的有机合成中间体。工业上用常用氯苯(C6H5Cl)和硫化氢(H2S)为主要原料制备苯硫酚,但会有副产物苯( C6H6)生成。
I:C6H5Cl(g)+H2S(g) C6H5SH(g)+HCl(g) △H1=-16.8kJ/mol
II:C6H5Cl(g)+H2S(g)===C6H6(g)+ HCl(g)+1/8S8(g) △H2
反应 II 的焓变不易测量,现查表得如下数据:
III: C6H5SH(g)=== C6H6(g)+1/8 S8(g) △H3=-29.0kJ/mol
④ △H2= __________________________
现将一定量的氯苯和硫化氢置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20分钟测定生成物的浓度,得到图二。
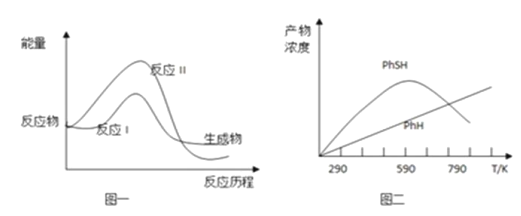
⑤ 上述反应 I、II 的能量变化如图一所示,则在相同条件下,反应速度 v(I)___ v( II)(填写“>”,“<”,“=”)。
⑥ 图二可知,790℃时所测生成物苯硫酚浓度减小,原因为_________
A.温度升高,平衡逆向移动 B.反应Ⅱ温度升高反应速率加快
⑦ 590℃时,2mol 氯苯和 5mol 硫化氢混合气体在 VL 的固定容积中进行反应 I 和II,达到平衡时,测得容器中苯硫酚的物质的量为 1mol,苯的物质的量为0.5mol,则该温度下反应 I 的平衡常数为_______。(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫是中学化学重要的非金属元素之一,请回答下列有关问题。
已知:2SO2(g)+O2(g)![]() 2SO3(g) △H=-196.6kJ/mol
2SO3(g) △H=-196.6kJ/mol
2NO(g)+O2(g)![]() 2NO2(g) △H=-113.0kJ/mol
2NO2(g) △H=-113.0kJ/mol
(1)反应NO2(g)+ SO2(g)![]() SO3(g)+NO(g)的ΔH= ______kJ/mol 。
SO3(g)+NO(g)的ΔH= ______kJ/mol 。
(2)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 _________。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO2的同时消耗1 molNO
(3)S2Cl2和SCl2均为重要的工业化合物。已知:
a.S2(l)+Cl2(g)![]() S2Cl2(g) △H1
S2Cl2(g) △H1
b.S2Cl2(g)+ Cl2(g)![]() 2SCl2(g) △H2
2SCl2(g) △H2
—定压强下,向10 L密闭容器中充入1 molS2Cl2和1 mol Cl2,发生反应b。Cl2与SCl2的消耗速率(υ)与温度(T)的关系如图所示:
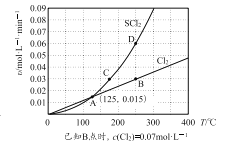
① A、B、C、D四点对应状态下,达到平衡状态的有______(填字母),理由是_______。
②—定温度下,在恒容密闭容器中发生反应a和反应b,达到平衡后缩小容器容积,重新达到平衡后,Cl2的平衡转化率_________(填“增大”或“减小”或“不变”),理由是________。
II.氮有不同价态的化合物,如氨、氮气、亚硝酸钠、乙二胺等。
图(I)和图(II)分别为二元酸H2A和乙二胺(H2NCH2CH2NH2)溶液中各微粒的百分含量δ(即物质的量百分数)随溶液pH的变化曲线(25℃)。
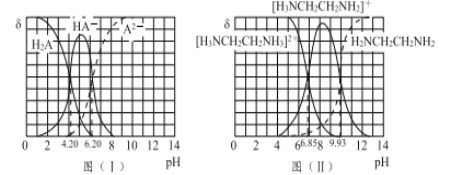
(1)H3NCH2CH2NH3A溶液显____(填“酸”或“碱”)性。
(2)乙二胺在水溶液中发生第二步电离的方程式:____________________,其平衡常数Kb2= _______________________ 。
(3)向20 mL 0.1 mol/L的H2A溶液加入10 mL 0.1 mol/L H2NCH2CH2NH2溶液后,溶液中各离子浓度大小的关系为 ____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com