
分析 ①氯化铁溶液和电路板上的铜反应生成氯化亚铁和氯化铜;
②红热的炭与浓硫酸加热反应生成二氧化硫和二氧化碳、水;
③过量的铁粉与稀硝酸反应,生成硝酸亚铁一氧化氮和水,根据电子守恒来配平方程式.
解答 解:①FeCl3溶液腐蚀电路板,Fe3+有强氧化性,能把金属铜氧化成铜离子,自身被还原成 Fe2+,离子方程式为:2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;
②红热的炭与浓硫酸反应的化学方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
③过量的铁粉与稀硝酸反应,生成硝酸亚铁,铁元素的化合价变化为0→+2,所以一个铁原子失去2个电子,氮元素的化合价变化为+5→+2,一个参加氧化还原反应的硝酸根离子得到3个电子,得失的最小公倍数是6,铁的计量数是3,NO的计量数是2,其它元素根据原子守恒进行配平,该方程式为:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O,
故答案为:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O.
点评 本题考查了方程式的书写,主要是反应条件,产物判断,过量的铁粉与稀硝酸反应,生成硝酸亚铁,为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32- | |
| B. | 向AgCl沉淀中滴入稀KI溶液白色沉淀变黄,说明AgI比AgCl更难溶 | |
| C. | 先加入盐酸无沉淀,再加入BaCl2溶液产生白色沉淀,则试样中一定有SO42- | |
| D. | 盐溶液中加入NaOH微热,产生使湿润的红色石蕊试纸变蓝的气体,则一定是铵盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V(NaOH)=0时,c(H+)=1×10-2mol•L-1 | |
| B. | V(NaOH)=10mL时,c(H+)=1×10-7mol•L-1 | |
| C. | V(NaOH)>10mL时,c(Na+)>c(C2O42-)>c(HC2O4-) | |
| D. | V(NaOH)<10mL时,不可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 焦炭在高温下与水蒸气的反应是吸热反应 | |
| B. | 燃料有足够的空气就能充分燃烧 | |
| C. | 氢氧化钾与硝酸的反应是放热反应 | |
| D. | 化学反应的过程,必定有能量的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液 | B. | Na2CO3溶液 | ||
| C. | 石蕊试液 | D. | 新制的Cu(OH)2悬浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
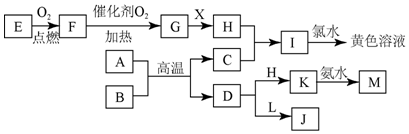
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 陈述 I | 陈述 II | 判断 | |
| A | SO2可使酸性高锰酸钾溶液腿色 | 因为SO2具有漂白性 | I对,II对,有 |
| B | 铁或铝制成的槽车可以密封贮运浓硫酸或浓硝酸 | 因为铁和铝不能与浓硝酸或浓硝酸反应 | I对,II对,无 |
| C | 铝箔在酒精灯火焰上,加热后熔化但液态铝不滴落 | 因为铝在空气中氧化生成一层薄薄的致密氧化膜,熔点高,而金属铝的熔点较低 | I对,II对,有 |
| D | 高压钠灯发出透雾性强的黄光 | 因为金属钠具有强还原性 | I对,II对,有 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com