
【题目】下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480 mL0.2 molL-1的稀硫酸。可供选用的仪器有:①托盘天平;②烧瓶;③烧杯;④药匙;⑤量筒;⑥玻璃棒。

(1)配制稀硫酸时,还缺少的仪器有________________(写仪器名称),
(2)下图是某些仪器的刻度部分示意图,其中为量筒的是________(填编号)。配制稀硫酸需要用量筒量取上述浓硫酸的体积为________mL,量取硫酸时应选用________(填选项)规格的量筒。
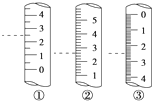
A.10mL B.50mL C.100mL D.200mL
(3)下图为量取浓硫酸后配制稀硫酸的操作示意图,其正确的操作步骤为_______(填编号)。
|
|
|
|
|
|
① | ② | ③ | ④ | ⑤ | ⑥ |
(4)对所配制的稀硫酸进行测定,发现其浓度大于0.2 mol/L,引起该误差的原因可能是_____。
A.所用的浓硫酸长时间放置在密封不好的容器中
B.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
C.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
D.将稀释后的稀硫酸未冷却立即转入容量瓶后,紧接着就进行以后的实验操作
E.定容时,俯视容量瓶刻度线进行定容
【答案】胶头滴管、500mL容量瓶 ② 5.4 A ⑤②⑥④①③ BDE
【解析】
(1)根据配制一定物质的量浓度的溶液的配制步骤选择使用的仪器和缺少的仪器;
(2)根据量筒的构造分析判断;先计算出浓硫酸的物质的量浓度,再根据溶液稀释定律c浓V浓=c稀V稀来计算;根据“大而近”的原则选择合适的量筒;
(3)根据配制一定物质的量浓度的溶液的配制步骤排序;
(4)根据c=![]() 并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析。
并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析。
(1)配制一定物质的量浓度的溶液的步骤为:计算、量取、溶解、冷却、转移、洗涤、定容、摇匀等,使用的仪器为:量筒、烧杯、玻璃棒、胶头滴管、容量瓶,配制480mL 0.2mol/L的稀硫酸,应选择500mL容量瓶,所以还缺少的仪器:胶头滴管;500mL容量瓶,故答案为胶头滴管、500mL容量瓶;
(2)量筒的刻度是从下而上标注的,而且没有0刻度,因此②为量筒;浓硫酸的物质的量浓度为c=![]() =
=![]() =18.4mol/L,设所需的浓硫酸的体积为VmL,根据溶液稀释定律c浓V浓=c稀V稀可知:18.4mol/L×VmL=0.2mol/L×500mL,解得V=5.4mL,故应选择10mL量筒,故答案为②;5.4;A;
=18.4mol/L,设所需的浓硫酸的体积为VmL,根据溶液稀释定律c浓V浓=c稀V稀可知:18.4mol/L×VmL=0.2mol/L×500mL,解得V=5.4mL,故应选择10mL量筒,故答案为②;5.4;A;
(3)配制一定物质的量浓度的溶液的步骤为:计算、量取、溶解、冷却、转移、洗涤、定容、摇匀等,因此量取浓硫酸后配制稀硫酸的操作顺序为⑤②⑥④①③,故答案为⑤②⑥④①③;
(4)A.所用的浓硫酸长时间放置在密封不好的容器中,浓硫酸被稀释浓度减小,则配制的溶液浓度偏低,故A不选;B.用量筒量取浓硫酸时,仰视刻度线,导致量取的浓硫酸体积偏大,硫酸的物质的量偏大,溶液浓度偏高,故B选;C.容量瓶用蒸馏水洗涤后未经干燥,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故C不选;D.将稀释后的稀硫酸立即转入容量瓶后,立即进行后面的实验操作,冷却后溶液体积偏小,溶液浓度偏高,故D选;E.定容时,俯视容量瓶刻度线,导致溶液体积偏小,溶液浓度偏高,故E选;故答案为BDE。


科目:高中化学 来源: 题型:
【题目】通过对阳极泥的综合处理可以回收贵重的金属,一种从铜阳极泥(主要成分为Se、Ag2Se、Ag、Cu、CuSO4和Cu2S等)中分离Ag、Se和Cu的新工艺流程如图所示:
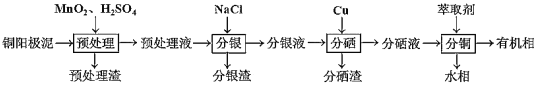
(1)已知预处理温度为80℃,预处理渣中几乎不含S元素,预处理时Cu2S发生反应的离子方程式为___,比起传统工艺中采用浓硫酸作氧化剂,本工艺中采用稀H2SO4溶液添加MnO2做预处理剂的主要优点是___。
(2)回收分渣中的银,可用如下过程:
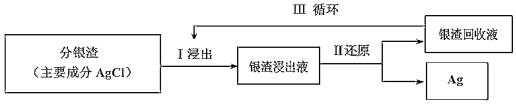
已知:S2O32-在碱性条件下很稳定,易与银离子络合:Ag++2S2O32-![]() Ag(S2O3)23-。常温下,络合反应的平衡常数为K稳[Ag(S2O3)23-]=2.8×1013,Ksp(AgCl)=1.8×10-10。
Ag(S2O3)23-。常温下,络合反应的平衡常数为K稳[Ag(S2O3)23-]=2.8×1013,Ksp(AgCl)=1.8×10-10。
①Ⅰ中发生的离子反应方程式为:AgCl(s)+2S2O32-(aq)![]() Ag(S2O3)23-(aq)+Cl-(aq),常温下此反应的平衡常数K为___(结果保留二位小数)。
Ag(S2O3)23-(aq)+Cl-(aq),常温下此反应的平衡常数K为___(结果保留二位小数)。
②Ⅱ中还原剂为Na2S2O4,在碱性条件下进行反应生成Na2SO3,相应的离子反应方程式为:2Ag(S2O3)23-+S2O42-+4OH-=2Ag+4S2O32-+2SO32-+2H2O,所以Ⅲ中的银渣回收液可直接循环使用,但循环多次后银的浸出率会降低,请从化学平衡移动的角度分析原因___。
(3)分硒渣的主要成分是Cu2Se,可被氧化得到亚硒酸(H2SeO3)。
①已知常温下H2SeO3的Ka1=2.7×10-3,Ka2=2.5×10-4,则NaHSeO3溶液的pH__7(填“>”、“<”或“=”)。
②二元强酸硒酸(H2SeO4)可以用电解亚硒酸溶液的方法制得,电解时的阳极反应式为___。
(4)分铜得到产品CuSO45H2O的具体操作如下:
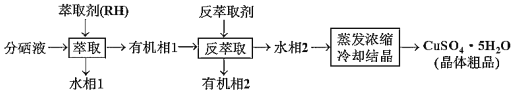
①萃取与反萃取原理为:2RH+Cu2+![]() R2Cu+2H+,反萃取剂最好选用__(填化学式)溶液。
R2Cu+2H+,反萃取剂最好选用__(填化学式)溶液。
②蒸发浓缩需用小火加热至溶液表面出现__为止,再冷却结晶即可得到产品CuSO45H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以某镍矿(主要成分为NiS、CuS、FeS、SiO2等)为原料制备一种多孔结构的细小镍晶粒,可用作有机物氢化反应的催化剂和储氢材料。工艺流程如图所示:[已知金属活动顺序为:Fe>Ni>(H)>Cu]
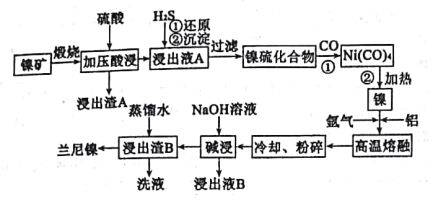
(1)已知该镍矿煅烧后生成Ni2O3,而加压酸浸液A中含有Ni2+,写出有关镍元素的加压酸浸的化学方程式___。
(2)已知Ni(CO)4的沸点是42.2℃,Ni(S)+4CO(g)![]() Ni(CO)4(g)的平衡常数与温度的关系如下:
Ni(CO)4(g)的平衡常数与温度的关系如下:

步骤①、步骤②的最佳温度分别是___、___(填选项代号)
A.25℃ B.30℃ C.50℃ D.80℃ E.230℃
(3)“高温熔融”时通入氩气的目的是___。
(4)“碱浸”是整个流程的核心步骤,该步骤的目的是___,发生反应的离子方程式为___。
(5)浸出液B可以回收,重新生成铝以便循环利用,请设计简单的回收流程:
(示例:![]() )浸出液B→___。
)浸出液B→___。
(6)镍硫化合物中会含有少量的CuS,也可以采用电解精炼的方法获得纯镍,流程为:
![]()
电解制粗镍时阳极发生的主要电极反应式为___;
精炼过程需控制pH2~5的原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物M的合成路线如下图所示:

已知:
(以上R、R’、R’’代表氢、烷基或芳基等)
(1)C中官能团名称为__________,B的化学名称为____________。
(2)F的结构简式为___________,则与F具有相同官能团的同分异构体共_____种(考虑顺反异构,不包含F)。
(3)由G生成H的化学方程式为________________________,反应类型为____________。
(4)下列说法正确的是________________(选填字母序号)。
a.由H生成M的反应是加成反应
b.可用硝酸银溶液鉴别B、C两种物质
c.1 mol E最多可以与4 mol H2发生加成反应
d.1 mol M与足量NaOH溶液反应,消耗4 mo1 NaOH
(5)以乙烯为起始原料,结合已知信息选用必要的无机试剂,写出合成CH3CH=CHCH3的路线________________ (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A.l mol硫酸钾中阴离子所带电荷数为NA
B.乙烯(C2H4)和环丙烷(C3H6)组成的28g混合气体中含有4NA个氢原子
C.22.4L氯气和足量氢气反应转移的电子数为2NA
D.将0.1mol氯化铁溶于1L水中,所得溶液含有0.2NA个Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色。下列正确的是
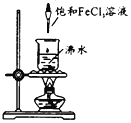
A.在暗处用激光笔照射液体,会出现一条光亮的通路
B.可用滤纸分离提纯得到氢氧化铁胶体
C.所得胶体中分散质的粒子直径大于100nm
D.取适量液体置于U型管,并通直流电,阳极颜色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是( )
A. H2+Cl2![]() 2HCl
2HCl
B. CuO+H2SO4=CuSO4+H2O
C. 2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
D. MgCl2+2NaOH=Mg(OH)2↓+2NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体NH4Br置于密闭容器中,在某温度下,发生反应:NH4Br(s)![]() NH3(g)+HBr(g),2HBr(g)
NH3(g)+HBr(g),2HBr(g)![]() Br2(g)+H2(g),2 min后,测知H2的浓度为0.5 mol·L-1,HBr的浓度为4 mol·L-1,若上述反应速率用v(NH3)表示,则下列速率正确的是( )
Br2(g)+H2(g),2 min后,测知H2的浓度为0.5 mol·L-1,HBr的浓度为4 mol·L-1,若上述反应速率用v(NH3)表示,则下列速率正确的是( )
A. 0.5 mol·L-1·min-1B. 2.5 mol·L-1·min-1
C. 2 mol·L-1·min-1D. 1.25 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示四种化学实验操作的名称按①②③④顺序排列分别为( )

A.过滤、蒸发、蒸馏、萃取(或分液或萃取分液)
B.过滤、蒸馏、蒸发、萃取
C.蒸发、蒸馏、过滤、萃取
D.萃取、蒸馏、蒸发、过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com