
分析 摩尔质量以g/mol为单位,数值上等于其相对分子质量,根据n=$\frac{N}{{N}_{A}}$计算硫酸的物质的量,氧原子物质的量为硫酸的4倍,H的物质的量为硫酸的2倍,根据m=nM计算H的质量.
解答 解:H2SO4的摩尔质量为98g/mol,1.204×1024个H2SO4分子物质的量为$\frac{1.204×1{0}^{24}}{6.02×1{0}^{23}}$=2mol,其中含有氧原子为2mol×4=8mol,H的物质的量为硫酸的2倍,则H的物质的量为4mol,H的质量为4mol×1g/mol=4g,
故答案为:98g/mol;2mol;8;4g.
点评 本题考查物质的量有关计算,比较基础,旨在考查学生对基础知识的巩固,侧重于考查学生的分析能力和计算能力.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:选择题
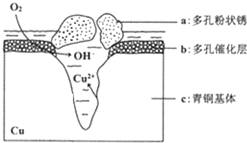 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义. 右图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.下列说法不正确的是( )
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义. 右图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.下列说法不正确的是( )| A. | 腐蚀过程中,负极是a | |
| B. | 正极反应是 O2+4e-+2H2O═4OH- | |
| C. | 若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为0.224L(标准状况) | |
| D. | 环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-═Cu2(OH)3Cl↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+2 O2 $\stackrel{点燃}{→}$ CO2+2H2O | |
| B. | CH2=CH2+H2 $\stackrel{催化剂}{→}$ CH3-CH3 | |
| C. |  +Br2 $\stackrel{FeBr_{3}}{→}$ +Br2 $\stackrel{FeBr_{3}}{→}$ +HBr +HBr | |
| D. | 2CH3CH2OH+O2 $→_{△}^{Cu或Ag}$ 2CH3CHO+2 H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 合成氨反应N2(g)+3H2(g)$?_{催化剂}^{高温高压}$ 2NH3(g)△H<0 具有重要的意义.
合成氨反应N2(g)+3H2(g)$?_{催化剂}^{高温高压}$ 2NH3(g)△H<0 具有重要的意义.| T/K | 473 | 573 | 673 | … |
| K | 4.4×10-2 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铜与盐酸、氢氧化钡与盐酸 | |
| B. | 石灰石和硝酸溶液、石灰石与盐酸溶液 | |
| C. | BaCO3与HCl溶液、Na2CO3溶液NaHSO4 | |
| D. | 石灰水中通CO2、石灰水中通SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙和稀盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 铁粉和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 向澄清石灰水中通入少量CO2:Ca2++2OH-+CO2═CaCO3↓+H2O | |
| D. | 硫酸铜溶液和氢氧化钡溶液混合:SO42-+Ba2+═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 | |
| B. | 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 | |
| C. | 蒸馏时蒸馏烧瓶中液体的体积不能超过其容积的规格,液体也不能蒸干 | |
| D. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com