
 2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心.水是组成生命体的重要化学物质,有关水的反应有很多.
2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心.水是组成生命体的重要化学物质,有关水的反应有很多.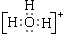 .
.分析 (1)两个水分子自身作用会生成阴、阳两种离子,阳离子为H3O+;
(2)水仅做氧化剂,则水中H元素的化合价降低;水既不做氧化剂又不做还原剂,则水中H、O元素的化合价均不变化;
(3)H2、O2和KOH的水溶液可形成氢氧燃料电池,负极上氢气失去电子;结合物质的量及2H2+O2=2H2O计算转移电子;
(4)①由信息可知镁离子的浓度最大为4.8mg/L;
②酸根离子的浓度最大为19.2mg/L.
解答 解:(1)两个水分子自身作用会生成阴、阳两种离子,阳离子为H3O+,其电子式为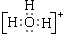 ,故答案为:
,故答案为: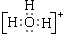 ;
;
(2)A.Cl2+H2O═HCl+HClO中,只有Cl元素的化合价变化,水既不是氧化剂也不是还原剂;
B.2Na2O2+2H2O═4NaOH+O2↑中,只有过氧化钠中O元素的化合价变化,水既不是氧化剂也不是还原剂;
C.CaH2+2H2O═Ca(OH)2+2H2↑中,水中H元素的化合价降低,则水为氧化剂;
D.3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2中,水中H元素的化合价降低,则水为氧化剂,
故答案为:CD;AB;
(3)H2、O2和KOH的水溶液可形成氢氧燃料电池,负极上氢气失去电子,负极反应为2H2+4OH--4e-=4H2O,得到1.8L饮用水时,水的物质的量为$\frac{1.8×10{\;}^{3}g}{18g/mol}$=100mol,由2H2+O2=2H2O中转移4e-可知,转移电子数为100mol×2×NA=200NA,故答案为:2H2+4OH--4e-=4H2O;200NA;
(4)①由信息可知镁离子的浓度最大为4.8mg/L,物质的量浓度为$\frac{\frac{4.8×10{\;}^{-3}}{24}}{1}$=2×10-4mol•L-1,故答案为:2×10-4mol•L-1;
②酸根离子的浓度最大为19.2mg/L,则500mL时硫酸根离子为0.5L×19.2mg/L=9.6mg,其物质的量为$\frac{9.6×10{\;}^{-3}g}{96g/mol}$=1×10-4mol,故答案为:1×10-4.
点评 本题考查较综合,涉及氧化还原反应、原电池及物质的量浓度的计算等,注重高频考点的考查,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定量的NaOH和Na2CO3的混合物,溶于水配成100mL溶液,然后用2mol•L-1的盐酸滴定(指示剂先为酚酞试剂,后用甲基橙试液),得到如图所示图象,回答下列问题:
一定量的NaOH和Na2CO3的混合物,溶于水配成100mL溶液,然后用2mol•L-1的盐酸滴定(指示剂先为酚酞试剂,后用甲基橙试液),得到如图所示图象,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去CO2中混有的少量SO2,可将气体通过装有酸性高锰酸钾溶液的洗气瓶 | |
| B. | 除去SiO2中混有的少量Al2O3,可选用NaOH溶液 | |
| C. | 除去溴苯中混有的少量苯,可加水后分液除去 | |
| D. | 乙酸乙酯中的少量乙酸和乙醇可通过氢氧化钠溶液除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 任何放热反应在常温条件下一定能发生 | |
| C. | 可以利用浓硫酸与氢氧化钠浓溶液反应来测定中和热 | |
| D. | 反应物和生成物具有的总能量的相对大小决定了反应是放热还是吸热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “洧水”的主要成分是油脂 | B. | “洧水”的主要成分是煤油 | ||
| C. | 烟的主要成分是炭黑 | D. | 烟的主要成分是石墨 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
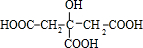 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图中A、B、C、D四条曲线分别表示IVA、VA、VIA、VIIA族元素的气态氢化物的沸点,其中表示VIA族元素气态氢化物沸点的是曲线( )
如图中A、B、C、D四条曲线分别表示IVA、VA、VIA、VIIA族元素的气态氢化物的沸点,其中表示VIA族元素气态氢化物沸点的是曲线( )| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 当开关K闭合后,电流计指针发生偏转,证明HCl是电解质 | |
| B. | 闭合开关K,往烧杯中加入NaCl固体,由于HCl与NaCl不反应,故电流计指针不发生变化 | |
| C. | 闭合开关K,往溶液中加入CaCO3固体,电流计示数显著增大 | |
| D. | 闭合开关K,往溶液中加入NaOH固体,电流计示数显著增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com