
【题目】关于二氧化硫和氯气的下列说法中正确的是
A. 都能使高锰酸钾溶液褪色B. 都能使溴水褪色
C. 都能使品红溶液褪色D. 都能使湿润红色布条褪色
科目:高中化学 来源: 题型:
【题目】甲醇来源丰富、价格低廉,是一种重要的化工原料,有着重要的用途和应用前景。
(1)工业生产甲醇的常用方法是:CO(g)+2H2(g) ![]() CH3OH(g) △H = —91kJ/mol。
CH3OH(g) △H = —91kJ/mol。
已知:2H2(g)+O2(g)=2H2O(l) △H = —580kJ/mol;
2CO(g)+O2(g)=2CO2(g) △H = —570kJ/mol
计算2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l) △H = ________________。
若在恒温恒容的容器内进行反应CO(g)+2H2(g) ![]() CH3OH(g),下列表示该反应没有达到平衡状态的有________(填字母序号)。
CH3OH(g),下列表示该反应没有达到平衡状态的有________(填字母序号)。
A.CO百分含量保持不变 B.容器中混合气体的密度不变化
C.有1个H—H键生成的同时有 3个C—H键生成 D.容器中混合气体的压强不变化
(2)制甲醇所需要的H2,可用下列反应制取:H2O(g)+CO(g) ![]() H2(g)+ CO2(g) △H<0,某温度下该反应达到平衡时,c(H2)·c(CO2)= c(CO)·c(H2O) 若起始时c(CO)=1mol/L-1,c(H2O)=1mol/L-1,试回答下列问题:
H2(g)+ CO2(g) △H<0,某温度下该反应达到平衡时,c(H2)·c(CO2)= c(CO)·c(H2O) 若起始时c(CO)=1mol/L-1,c(H2O)=1mol/L-1,试回答下列问题:
①该温度下,反应进行一阶段时间后,测得H2的浓度为0.5mol/L-1,则此时该反应v(正)__________v(逆)(填“>”、“<”或“=”);
②若反应温度不变,达到平衡后,H2O的转化率为________。
(3)某实验小组设计了甲醇以氢氧化钾为电解质溶液的燃料电池装置。
①试想该电池工作时,OH— 向_______极移动(填“负”或“正”);
②工作一段时间后,测得溶液的pH减小,该电池负极反应的离子方程式为______________________。总反应的化学方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是
A. 足量乙酸与碳酸钠溶液反应: 2 CH3COOH +CO32-→ 2CH3COO-+CO2↑+H2O
B. 醋酸溶液与新制氢氧化铜反应: 2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O
C. 苯酚钠溶液中通入少量二氧化碳: 2C6H5O-+CO2+H2O→2C6H5OH+CO32-
D. 乙醛溶液与足量的银氨溶液共热CH3CHO+2[Ag(NH3)2]++2OH-![]() CH3COO-+NH4++2Ag↓+3NH3+H2O
CH3COO-+NH4++2Ag↓+3NH3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应2 A![]() B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(molL-1)随反应时间(min)的变化情况如下表所示。
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(molL-1)随反应时间(min)的变化情况如下表所示。
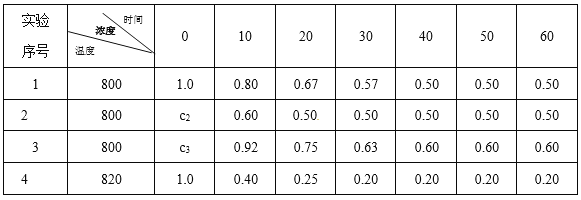
根据上述数据,完成下列填空:
(1)在实验1中,反应在10~20 min时间内A的平均反应速率为___________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c2=________mol·L-1。
(3)设实验3的反应速率为v3。,实验1的反应速率为v1,则v3_____vl(填“>”、“="或“<”)。
(4)比较实验4和实验1,可推测该反应是_______(填“吸热”或“放热”)反应。
理由是_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)中国古代四大发明之一黑火药,它的爆炸反应为2KNO3+3C+S =A + N2↑ +3CO2↑(已配平)
①除S外,上述反应中所涉及到的非金属元素的电负性从大到小顺序依次为_____________,K2O,CO2,SO2,SiO2四种晶体的熔点由高到低的顺序______________________
②生成物A的电子式为_____________。推算HCN分子中![]() 键与
键与![]() 键数目之比为_______________。
键数目之比为_______________。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多 2。T在元素周期表中的位置为__________________,1molQ2+的未成对电子数是__________个。
(3)在![]() 的水溶液中,一定条件下存在组成为
的水溶液中,一定条件下存在组成为![]() (n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
[CrCln(H2O)6-n]x+ + xR-H = Rx[CrCln (H2O)6-n] + xH+
交换出来的H+经中和滴定,即可求出x和n,从而确定配离子的组成。
将含0.0015 mol ![]() 的溶液,与R-H完全交换后,中和交换过程中生成的H+需浓度为0.1200 mol·L-1 的NaOH溶液25.00 ml,则该配离子的化学式为_________________________。
的溶液,与R-H完全交换后,中和交换过程中生成的H+需浓度为0.1200 mol·L-1 的NaOH溶液25.00 ml,则该配离子的化学式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G( ![]() )是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
)是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
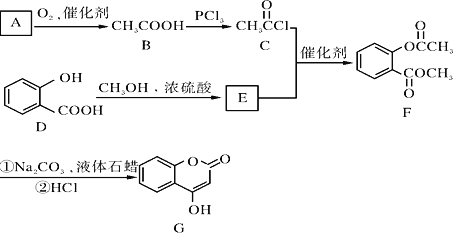
(1)A与银氨溶液反应有银镜生成,则A的结构简式是____________,D中官能团名称为_________________B→C的反应类型是________反应。
(2)下列关于G的说法不正确的是__________(填字母)。
A.能与溴的四氯化碳溶液反应 b.能与金属钠反应
C.1molG最多能和5mol氢气反应 d.分子式是C9H6O3
(3)写出满足下列条件的E的同分异构体的结构简式:___________________。
①苯环上的一氯取代产物只有一种;
②能发生银镜反应;
③能与FeCl3溶液发生显色反应。
(4)写出F和过量NaOH溶液共热时反应的化学方程式:_____________。
(5)请利用上述框图中的反应设计合理的方案,以苯酚和乙醇为原料合成乙酸苯酯![]() (用合成路线流程图表示,并注明反应条件).
(用合成路线流程图表示,并注明反应条件).
提示:①合成过程中无机试剂任选;②合成路线流程图示例如下:
CH3CH2OH![]() H2C=CH2
H2C=CH2![]() BrH2C-CH2Br.
BrH2C-CH2Br.
___________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃基异构化是当前环保的急切要求,正戊烷异构化为异戊烷的热化学方程式是: CH3CH2CH2CH2CH3![]() CH3CH(CH3)CH2CH3 △H=-7.1 kJ·mol-1
CH3CH(CH3)CH2CH3 △H=-7.1 kJ·mol-1
(1)正戊烷异构化反应选择的温度条件是____________。
(2)由于副反应较为复杂,提髙产率的最佳方法是____________。
(3)如果提高温度,反应速率___________,转化率___________(填“升高"“不变”或“降低” ),同时还会产生积炭现象,假如在反应物中掺入一定量水,则可以减弱这种现象,理由是___________(用化学方程式表示)。
(4)在573 K时,正戊烧转化率为54%,则此时平衡常数为___________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352 g,置于铂舟并放入燃烧管中,不断通入氧气流。用酒精喷灯持续加热样品,将生成物先后通过浓硫酸和碱石灰,两者分别增重0.144 g和0.528 g,生成物完全被吸收。试回答以下问题:
(1)维生素C中碳的质量分数是_____________,氢的质量分数____________
(2)维生素中是否含有氧元素?为什么?(试通过计算说明)
(3)如果需要你确定维生素C的分子式,你还需要哪些信息?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置 如右下图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1︰2,以下说法不正确的是

A. a极与电源的正极相连
B. 产物丙为硫酸溶液
C. 离子交换膜d为阳离子交换膜(允许阳离子通过)
D. a电极反应式为2H2O+2e-=2OH-+ H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com