
用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol·L-1FeCl3溶液,可制得一种红褐色胶体。
(1)反应的化学方程式为____________________________________________________。
(2)如何用较简单的方法判断胶体是否制备成功?
________________________________________________________________________。
(3)向该胶体中逐滴加入盐酸,会出现一系列变化:
①先出现红褐色沉淀,原因是________________________________________________。
②随后红褐色沉淀溶解,此反应的离子方程式是________________________________。
科目:高中化学 来源: 题型:
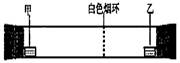
已知气体的摩尔质量越小,扩散速度越快。 右图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的判断正确的是( )
A.甲是浓氨水,乙是浓硫 B.甲是浓盐酸,乙是浓氨水
C.甲是浓氨水,乙是浓盐酸 D.甲是浓硝酸,乙是浓氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的叙述正确的是
A.分液时分液漏斗的下端与过滤时漏斗的下端均要贴紧烧杯内壁,其原因相同
B.配制一定物质的量浓度溶液时,在溶解、移液、洗涤、定容时均要用到玻璃棒
C.浓硫酸和浓氢氧化钠溶液溅到皮肤上,均应马上用大量的水冲洗,以防腐蚀皮肤
D.不用其它试剂,只用胶头滴管和试管即可鉴别出NaHCO3、Ba(OH)2、稀H2SO4三种溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分。
(1)Cu2+基态的电子排布式可表示为 ;
(2)SO42-的空间构型为 (用文字描述);中心原子采用的轨道杂化方式是 ;写出一种与SO42-互为等电子体的分子的化学式: ;
(3) 向CuSO4 溶液中加入过量NaOH溶液可生成[Cu (OH)4 ]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为 ;
(4)资料显示ZnS为难溶物,在活化过程中,CuSO4能转化为CuS的原因是 。
(5)CuS比CuO的熔点 (填高或低),原因是 。
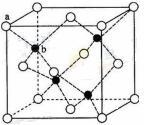
(6)闪锌矿的主要成分ZnS,晶体结构如下图所示,其晶胞边长为540.0 pm,密度为____________(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为___________________pm(列式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法在一定条件下可以实现的是( )。
①酸性氧化物与碱发生反应
②弱酸与盐溶液反应可以生成强酸
③没有水生成,也没 有沉淀和气体生成的复分解反应
有沉淀和气体生成的复分解反应
④两种酸溶液充分反应后的溶液体系为中性
⑤有单质参加的非氧化还原反应
⑥两种氧化物反应的产物有气体
A.①②③④⑤⑥ B.②④⑤⑥
C.①②③⑤ D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
①1 mol某链烃最多能和2 mol HCl发生加成反应,生成1 mol氯代烷;②1 mol该氯代烷能和8 mol Cl2发生取代反应,生成只含碳元素和氯元素的氯代烃。该链烃可能是 ( )。
A.CH3CH===CH2  B.CH2===CHCH===CH2
B.CH2===CHCH===CH2
C.CH3CH===CHCH3 D.CH3C≡CH
查看答案和解析>>
科目:高中化学 来源: 题型:
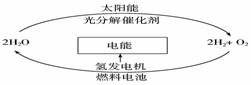 科学家预测“氢能”将是人类社会最理想的新能源,目前,有人提出一种最经济最理想的获得氢能源的循环体系,如下图所示。下列说法错误的是 ( )
科学家预测“氢能”将是人类社会最理想的新能源,目前,有人提出一种最经济最理想的获得氢能源的循环体系,如下图所示。下列说法错误的是 ( )
A.在氢能的利用过程中,H2O可循环使用
B.氢气、氧气和稀硫酸构成的燃料电池中,正极的电极反应为:O2 + 4e- + 2H2O = 4OH-
C.该法制氢的关键是寻找光分解催化剂
D.利用光电转化可将太阳能转化为电能用于电解水而获得氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
在400℃,1.01X105Pa时,将SO2和14molO2 压入一个装有催化剂的VL密闭反应器中,发生2SO2+O2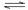 2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2
2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2
(1)SO2的起始浓度为_________,SO3(g)的平衡浓度为_________;
(2)SO2的转化率为_________,O2的平均反应速率为_________;
(3)平衡时SO3占总体积的百分数为________________,
此时体系压强为反应起始时体系压强的________倍;
(4)达平衡后再加入2molSO2、12molO2和4molSO3(g),此时正反应速率将__________,
逆反应速率将__________(填“增大”,“减小”或“不变”),平衡__________移动(填“向左”,“向右”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
 I是常规核裂变产物之一,可以通过测定大气或水中
I是常规核裂变产物之一,可以通过测定大气或水中 I的含量变化来检测核电站是否发生放射性物质泄漏。下列有关
I的含量变化来检测核电站是否发生放射性物质泄漏。下列有关 I的叙述中错误的是 ( )
I的叙述中错误的是 ( )
A.  I与
I与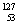 I 互为同位素 B.
I 互为同位素 B.  I的质子数为53
I的质子数为53
C.  I的原子核外电子数为78 D.
I的原子核外电子数为78 D.  I的原子核内中子数多于质子数
I的原子核内中子数多于质子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com