
【题目】将SO2气体通入BaCl2溶液,无沉淀生成,再通入X气体,有沉淀生成,则X不可能是
A.Cl2B.H2SC.NH3D.CO2
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
【题目】据报道,氢燃料电池公交汽车已经驶上北京街头,下列说法中,正确的是
A. 电解水制取氢气是理想而经济的制氢方法
B. 发展氢燃料电池汽车不需要安全高效的储氢技术
C. 氢燃料电池汽车的使用可以有效减少城市空气污染
D. 氢燃料电池把氢气和氧气燃烧放出的热能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列AI九种中学化学常见的物质之间的转化关系如图所示。已知A为固态非金属单质,B 在实验室常用作气体干燥剂,D为常见液体,常温下C、E、F都是无色气体,E能使酸性高锰酸钾溶液褪色,G是侯氏制碱法的最终产品

回答下列问题:
(1)F的分子式是________________,图中淡黄色固体中的阴、阳离子个数比为____________。
(2)A与B反应的化学方程式是:___________________________________________________。
(3)E转变为H和I的离子方程式是___________________________________________________。
(4)简述检验I溶于水电离所产生的阴离子的操作方法、实验现象和结论: ____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表为短周期的一部分,推断关于Y,Z,M的说法正确的是( ) 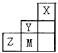
A.非金属性:Y>Z>M
B.原子半径:M>Z>Y
C.气态氢化物的稳定性:Y<M<Z
D.ZM2分子中各原子的最外层均满足8e﹣稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有4种碳骨架如下的烃,下列说法正确的是( ) ![]()
①a和d是同分异构体
②b和c是同系物
③a和d都能发生加聚反应
④只有b和c能发生取代反应.
A.①②
B.①④
C.②③
D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z均为短周期元素,X元素的气态氢化物通入无色酚酞溶液,溶液变红,Y元素的最外层电子数是次外层电子数的3倍,Z元素是短周期元素中原子半径最大的元素(He、Ne、Ar除外).
(1)Z元素的最高价氧化物对应的水化物的电子式为;
(2)X元素与Y元素最简单的气态氢化物的热稳定性顺序为;
(3)Y元素的最简单氢化物和Z元素的过氧化物发生氧化还原反应的化学方程式为 .
(4)碱性条件下,X元素的气态氢化物和单质Y2可形成原电池,正极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各原子或离子的电子排布式正确的是( )
A.O2-:1s22s22p6B.Na+:1s22s22p63s1
C.Al:1s22s22p63s2D.Si:1s22s22p63s23p4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验.甲同学:向1molL﹣1的FeCl3溶液中加少量NaOH溶液.乙同学:直接加热饱和FeCl3溶液.丙同学:向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热.
试回答下列问题:
a.其中操作正确的同学是 .
b.证明有Fe(OH)3胶体生成的实验操作是 .
c.已知同种胶体微粒带有同种电荷,丁同学将所制得的Fe(OH)3胶体装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变深,这表明Fe(OH)3胶体微粒带(带“正”或“负”)电荷.
(2)某学生欲用98% (ρ=1.84g/cm3)的硫酸配制6.0mol/L的H2SO4溶液950mL,请回答下列问题:
d.实验所用98%的硫酸的物质的量浓度为mol/L.
e.该实验需要使用到的玻璃仪器有:量筒、烧杯、玻璃棒、胶头滴管、 .
f.若配制操作定容时,眼睛俯视,则所配制的溶液浓度将(偏大、偏小,无影响?)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com