
”¾ĢāÄæ”æĀĮŗĻ½š”¢Ńõ»ÆĀĮ”¢ĮņĖįĀĮČżÖÖĪļÖŹµÄ·ÖĄąÕżČ·µÄŹĒ£Ø £©
A.»ģŗĻĪļ”¢Ńõ»ÆĪļ”¢ŃĪ
B.µ„ÖŹ”¢»ģŗĻĪļ”¢ŃĪ
C.ŃĪ”¢Ńõ»ÆĪļ”¢“æ¾»Īļ
D.»ģŗĻĪļ”¢ŃĪ”¢»ÆŗĻĪļ
”¾“š°ø”æA
”¾½āĪö”æ½ā£ŗA”¢ĀĮŗĻ½šŹĒ½šŹōĀĮÓėĘäĖū½šŹō»ņ·Ē½šŹō³É·ÖøßĪĀČŪŗĻ¶ų³É£¬ŹōÓŚ»ģŗĻĪļ£»Ńõ»ÆĀĮŹōÓŚŃõ»ÆĪļ£¬ĮņĖįĀĮŹōÓŚŃĪ£¬¹ŹAÕżČ·£» B”¢ĀĮŗĻ½šŹĒ½šŹōĀĮÓėĘäĖū½šŹō»ņ·Ē½šŹō³É·ÖøßĪĀČŪŗĻ¶ų³É£¬ŹōÓŚ»ģŗĻĪļ£¬²»ŹĒµ„ÖŹ£¬Ńõ»ÆĀĮŹōÓŚŃõ»ÆĪļ£¬¹ŹB“ķĪó£»
C”¢ĀĮŗĻ½šŹĒ½šŹōĀĮÓėĘäĖū½šŹō»ņ·Ē½šŹō³É·ÖøßĪĀČŪŗĻ¶ų³É£¬ŹōÓŚ»ģŗĻĪļ£¬²»ŹōÓŚŃĪ£¬¹ŹC“ķĪó£»
D”¢Ńõ»ÆĀĮŹōÓŚŃõ»ÆĪļ£¬²»ŹōÓŚŃĪ£¬¹ŹD“ķĪó£»
¹ŹŃ”A£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹŹōÓŚŗĻ³ÉĻĖĪ¬µÄŹĒ£Ø””””£©
A. ÓŠ»ś²£Į§ B. ½õĀŚ C. µēľ D. °¢½ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼īŹ½Ģ¼ĖįĆ¾ŗĶĪŽĖ®ĀČ»ÆĆ¾¾ßÓŠ¹ć·ŗµÄÓĆĶ¾”£ÓĆ°×ŌĘŹÆ(CaCO3”¤MgCO3)ĪŖÖ÷ŅŖŌĮĻÉś²ś¼īŹ½Ģ¼ĖįĆ¾ŗĶĪŽĖ®ĀČ»ÆĆ¾µÄĮ÷³ĢČēĻĀ£ŗ
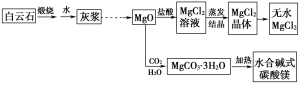
»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)”°»Ņ½¬”±ÖŠ³żĖ®ŗĶMgOĶā£¬Ö÷ŅŖ³É·Ö»¹ÓŠ________________________”£
(2)ĪŖĢ½¾æĖłµĆµÄĖ®ŗĻ¼īŹ½Ģ¼ĖįĆ¾[mMgCO3”¤nMg(OH)2”¤xH2O]µÄ×é³É£¬Ä³Ķ¬Ń§×é×°ŅĒĘ÷ČēĶ¼ĖłŹ¾£ŗ
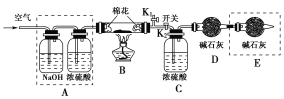
ŹµŃé²āµĆ£ŗÓ²ÖŹ²£Į§¹ÜÖŠŹ£ÓąµÄ¹ĢĢåÖŹĮæĪŖ1.60 g£¬C“¦ÅØH2SO4ŌöÖŲ0.72 g£¬D“¦¼īŹÆ»Ņ(Ö÷ŅŖ³É·ÖĪŖŃõ»ÆøĘŗĶĒāŃõ»ÆÄĘ)ŌöÖŲ1.32 g£¬“ĖĖ®ŗĻ¼īŹ½Ģ¼ĖįĆ¾µÄ»ÆѧŹ½ĪŖ________”£
(3)Aæņ֊װÖƵÄ×÷ÓĆŹĒ___________________________________________£»ŌŚ×°ŗĆŹŌ¼Įŗ󣬼ÓČČĒ°Ó¦½ųŠŠµÄ²Ł×÷ŹĒ_______________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶس£¼ģ²āSO2ŗ¬ĮæŹĒ·ń“ļµ½Åŷűź×¼µÄ·“Ó¦ŌĄķŹĒSO2 +H2O2 + BaCl2 ===BaSO4”ż+ 2HCl”£NA±ķŹ¾°¢·üŁ¤µĀĀŽ³£Źż£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. 0.1 mol BaCl2¾§ĢåÖŠĖłŗ¬Ī¢Į£×ÜŹżĪŖ0.1NA
B. 25 ”ꏱ£¬pH =1µÄHClČÜŅŗÖŠŗ¬ÓŠH+µÄŹżÄæĪŖ0.1NA
C. 17 g H2O2ÖŠŗ¬ÓŠ·Ē¼«ŠŌ¼üŹżÄæĪŖ0.5NA
D. Éś³É2.33 g BaSO4³ĮµķŹ±£¬×ŖŅʵē×ÓŹżÄæĪŖ0.01NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»¶ØĪĀ¶ČĻĀ£¬AgCl ÓėAgIµÄ±„ŗĶČÜŅŗÖŠ“ęŌŚČēĻĀ¹ŲĻµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
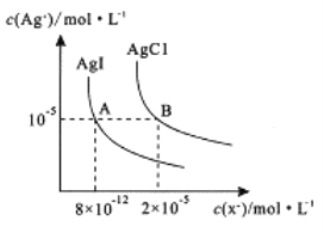
A. AgCl(s) +I-(aq)![]() AgI(s) +Cl-(aq)£¬ŌŚøĆĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżK=2.5”Į106
AgI(s) +Cl-(aq)£¬ŌŚøĆĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżK=2.5”Į106
B. Ļņ0.1mol/LKIČÜŅŗÖŠ¼ÓČėAgNO3 ČÜŅŗ£¬µ±I-øÕŗĆĶźČ«³ĮµķŹ±£¬c(Ag+ )=2”Į10-12mol/L
C. ĻņAgCl”¢AgIµÄ±„ŗĶČÜŅŗÖŠ¼ÓČėĒāµāĖįČÜŅŗ£¬æÉŹ¹ČÜŅŗÓÉAµć±äµ½Bµć
D. Ļņ2 mL0.01mol/LAgNO3£¬ČÜŅŗÖŠ¼Ó¼øµĪ0.01mol/L NaC1ČÜŅŗ£¬¾²ÖĆʬæĢ£¬ŌŁĻņČÜŅŗÖŠ¼Ó¼øµĪ0.01mol/LKIČÜŅŗ£¬ÓŠ»ĘÉ«³ĮµķÉś³É£¬ĖµĆ÷Ksp(AgCl)>Ksp(AgI)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌĻĀĮŠŹµŃéĻÖĻó¼°Ęä½āŹĶ²»ÕżČ·µÄŹĒ
A. ½šŹōÄĘŌŚCl2ÖŠČ¼ÉÕ²śÉś°×ŃĢ£¬ÕāŹĒŅņĪŖ²śÉśµÄNaCl¹ĢĢåæÅĮ£·ÖÉ¢µ½æÕĘųÖŠĖłÖĀ
B. °ŃÉÕŗģµÄĢśĖæ·ÅŌŚŃõĘųÖŠ£¬·¢³öŅ«ŃŪ°×¹ā£¬²śÉśŗŚÉ«¹ĢĢ壬ÕāŹĒŅņĪŖøĆ·“Ó¦·ÅČȶą£¬Éś³ÉµÄFe3O4ĪŖŗŚÉ«
C. µ„ÖŹMg”¢AlÓėO2·“Ó¦£¬Ģõ¼ž²»Ķ¬£¬æÉÄܲśÉś²»Ķ¬µÄ²śĪļ
D. Ć¾“ųŌŚæÕĘųÖŠµćČ¼·¢³öŅ«ŃŪ¹āĆ¢£¬²¢·¢ÉśČżøö·“Ó¦£ŗ2Mg£«O2![]() 2MgO”¢3Mg£«N2
2MgO”¢3Mg£«N2![]() Mg3N2”¢2Mg£«CO2
Mg3N2”¢2Mg£«CO2![]() 2MgO£«C(ŗŚÉ«)£¬Mg³£ÓĆÓŚÕÕĆ÷µÆ”£ŌŚÕāŠ©·“Ó¦ÖŠ£¬Mg¶¼ŹĒ×÷»¹Ō¼Į
2MgO£«C(ŗŚÉ«)£¬Mg³£ÓĆÓŚÕÕĆ÷µÆ”£ŌŚÕāŠ©·“Ó¦ÖŠ£¬Mg¶¼ŹĒ×÷»¹Ō¼Į
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢśĢ¼Ī¢µē½ā¼¼ŹõŹĒĄūÓĆŌµē³ŲŌĄķ“¦ĄķĖįŠŌĪŪĖ®µÄŅ»ÖÖ¹¤ŅÕ£¬×°ÖĆČēĶ¼”£ČōÉĻ¶ĖæŖæŚ¹Ų±Õ£¬æɵƵ½Ē滹ŌŠŌµÄH+£ØĒāŌ×Ó£©£»ČōÉĻ¶ĖæŖæŚ“ņæŖ£¬²¢¹ÄČėæÕĘų£¬æɵƵ½ĒæŃõ»ÆŠŌµÄ”¤OH£ØĢž»ł×ŌÓÉ»ł£©”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ

A. ĪŽĀŪŹĒ·ń¹ÄČėæÕĘų£¬øŗ¼«µÄµē¼«·“Ó¦Ź½¾łĪŖFe-2e-=Fe2+
B. ²»¹ÄČėæÕĘųŹ±£¬Õż¼«µÄµē¼«·“Ó¦Ź½ĪŖH++e-=H”¤
C. ¹ÄČėæÕĘųŹ±£¬ĆæÉś³É1mol”¤OHÓŠ2molµē×Ó·¢Éś×ŖŅĘ
D. “¦Ąķŗ¬ÓŠ²ŻĖį£ØH2C2O4£©µÄĪŪĖ®Ź±£¬ÉĻ¶ĖæŖæŚÓ¦“ņæŖ²¢¹ÄČėæÕĘų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲĪļÖŹŠŌÖŹ»ņÓĆĶ¾µÄĖµ·Ø²»ÕżČ·µÄŹĒ
A.³£ĪĀĻĀÅØĮņĖįæÉÖü“ęŌŚĢś¹ŽÖŠ
B.ClO2¾ßÓŠŃõ»ÆŠŌ£¬æÉÓĆÓŚ×ŌĄ“Ė®µÄɱ¾śĻū¶¾
C.Č¼×ŵÄĆ¾Ģõ·ÅČėŹ¢Āś¶žŃõ»ÆĢ¼µÄ¼ÆĘųĘæÖŠæɼĢŠųČ¼ÉÕ
D.Ģś±ČĶ½šŹōŠŌĒ棬ĖłŅŌæÉÓĆFeCl3øÆŹ“CuæĢÖĘÓ”Ė¢µēĀ·°å
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©ĀČ»Æļ§µÄĖ®ČÜŅŗĻŌČõĖįŠŌ£¬ĘäŌŅņĪŖ___________________(ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾)£¬0.1 molL-1µÄ°±Ė®ÖŠ¼ÓČėÉŁĮæµÄNH4Cl¹ĢĢ壬ČÜŅŗµÄpH________(Ģī”°Éżøß”±»ņ”°½µµĶ”±)£»Čō¼ÓČėÉŁĮæµÄĆ÷·Æ£¬ČÜŅŗÖŠµÄNH4+µÄÅضČ__________(Ģī”°Ōö“ó”±»ņ”°¼õŠ””±)£»
£Ø2£©25”ę£¬Į½ÖÖĖįµÄµēĄėĘ½ŗā³£ŹżČēĻĀ±ķ”£
»ÆѧŹ½ | CH3COOH | H2CO3 | HCN | HClO | H2SO3 |
µēĄė³£Źż | 1.8”Į10£5 | K1£½4.3”Į10£7 K2£½5.6”Į10£11 | 5”Į10-10 | 3.0”Į10£8 | K1=2”Į10-2 K2=1”Į10-7 |
¢ŁĪļÖŹµÄĮæÅØ¶Č¾łĪŖ0.1 mol/LµÄĖÄÖÖČÜŅŗ£ŗ
a£®CH3COONa b£®Na2CO3 c£®NaClO d£®NaHCO3
pHÓɓ󵽊”µÄĖ³ŠņĪŖ__________£ØÓƱąŗÅĢīŠ“£©”£
¢Śøł¾ŻÉĻ±ķŹż¾ŻÅŠ¶Ļ£¬ĻĀĮŠĄė×Ó·½³ĢŹ½“ķĪóµÄŹĒ__________”£
A£®CO2(¹żĮæ)+H2O+ClO-=HCO3-+HClO B£®SO2(¹żĮæ)+H2O+ClO-=HSO3-+HClO
C£®CO2(ÉŁĮæ)+H2O+CN-=HCO3-+HCN D£®SO2(ÉŁĮæ)+H2O+CN-=HSO3-+HCN
E£®SO2(ÉŁĮæ)+2CO32-+H2O=SO32-+2HCO3- F£®2SO2(¹żĮæ)+CO32-+H2O=2HSO3-+CO2”ü
¢Ū0.10 molL-1Na2SO3ČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņĪŖ___________________”£
¢Ü25”ꏱ£¬NaCNÓėHCNµÄ»ģŗĻČÜŅŗ£¬Čōc£ØCN-£©=c£ØHCN£©£¬ŌņČÜŅŗÖŠpH=__________£ØŅŃÖŖlg2=0.3£¬lg5=0.7£©”£
¢Ż25”ꏱ£¬ČōĻņNaHSO3ČÜŅŗÖŠ¼ÓČėÉŁĮæµÄI2£¬ŌņČÜŅŗÖŠ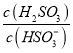 ½«__________£ØĢī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±£©”£
½«__________£ØĢī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±£©”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com