
【题目】NaClO溶液是一种纺织工业用漂白剂,可用一定比例NaOH、Na2CO3的混合溶液和Cl2反应制备。
(1)NaHCO3的存在能增强NaClO溶液的稳定性。Cl2与混合溶液中Na2CO3反应制备NaClO,同时生成NaHCO3,其化学方程式为___。
(2)NaClO溶液中若含有NaClO3会影响产品的品质。测定碱性NaClO样品中NaClO3物质的量浓度的方法如下:取20.00mLNaClO溶液试样,加入过量H2O2,充分反应后,加热煮沸,冷却至室温,加入硫酸酸化,再加入0.1000mol·L-1FeSO4标准溶液30.00mL,充分反应后,用0.01000mol·L-1酸性K2Cr2O7溶液滴定过量的FeSO4溶液至终点(Cr2O72-被还原为Cr3+),消耗该溶液25.00mL。
已知:ClO3-在碱性条件下性质稳定,在酸性条件下表现出强氧化性;ClO3-+Fe2++H+—Cl-+Fe3++H2O(未配平)。
①加入过量H2O2的目的是__。
②实验中若缺少加热煮沸步骤,所测NaClO3物质的量浓度会有较大误差,原因可能是___(答出一个即可)。
③计算样品中NaClO3物质的量浓度___(写出计算过程)。
【答案】2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3 将NaClO完全还原 NaClO3在酸性条件下被过量的H2O2还原或部分硫酸亚铁被过量H2O2氧化 1.250×10-2mol·L-1
【解析】
(1)根据题意,反应物为Na2CO3、Cl2、H2O,其中Cl2、H2O反应产生HCl和HClO,都可以与Na2CO3反应,故产物有NaClO、NaHCO3、NaCl。方程式为:2Na2CO3+Cl2+H2O= NaClO+NaCl+2NaHCO3;
(2)①由于NaClO也有强氧化性,会影响NaClO3的测定,所以开始时加H2O2是为了将NaClO完全还原,避免跟后面加入的还原剂Fe2+反应,影响实验结果;
②加热煮沸主要目的是让H2O2分解。若H2O2有剩余,则可能跟酸性条件下NaClO3的反应,或者跟Fe2+反应,使结果出现误差;
③根据题意,Fe2+既与K2Cr2O7反应,又与NaClO3反应。Fe2+的物质的量为0.1mol/L×0.03L=0.003mol, K2Cr2O7的物质的量为:0.01mol/L×0.025L =0.00025mol。由电子转移守恒可得![]() ,则与Cr2O72-反应的Fe2+的物质的量为0.00025mol×6=0.0015mol,那么与ClO3-反应的Fe2+的物质的量为0.003mol-0.0015mol=0.0015mol,根据电子转移守恒可得
,则与Cr2O72-反应的Fe2+的物质的量为0.00025mol×6=0.0015mol,那么与ClO3-反应的Fe2+的物质的量为0.003mol-0.0015mol=0.0015mol,根据电子转移守恒可得![]() ,则ClO3-的物质的量为0.0015mol÷6=0.00025mol,所以NaClO3物质的量浓度c=
,则ClO3-的物质的量为0.0015mol÷6=0.00025mol,所以NaClO3物质的量浓度c=![]() 。
。


科目:高中化学 来源: 题型:
【题目】制取乙烯时,常因温度过高而发生副反应,部分乙醇跟浓H2SO4 反应生成SO2,CO2,水蒸气和炭黑。
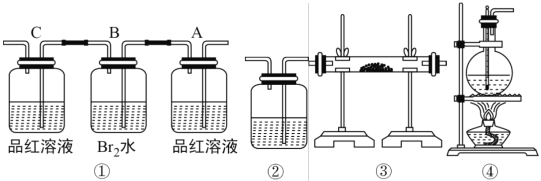
(1)用编号为①→④的实验装置设计一个实验,以验证上述反应混合气体中含CO2,SO2和水蒸气。写出装置的连接顺序(按产物气流从左到右的流向填写编号):______。
(2)实验的装置①中 A 瓶的现象是______;结论为__________。 B 瓶中的现象是__________; B 瓶溶液作用为__________。若 C 瓶中品红溶液不褪色,可得到结论为__________。
(3)装置③中加的固体药品是______以验证混合气体中有______。装置②中盛的溶液是_____以验证混合气体中有______。
(4)简述装置①在整套装置中位置的理由__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种制氢技术原理如图所示。容器Ⅰ中发生的某反应a为C(s)+2H2O(g)![]() CO2(g)+2H2(g);ΔH。下列有关说法正确的是( )
CO2(g)+2H2(g);ΔH。下列有关说法正确的是( )
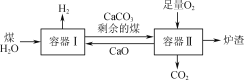
A.已知反应a在一定条件下能够自发进行,则该反应的ΔH<0
B.向容器Ⅰ中加入CaO能有效实现H2与CO2的分离
C.剩余的煤进入容器Ⅱ是为了充分利用其与O2反应放出的热量
D.煤中含有的S在容器Ⅱ中最终转化为CaSO3进入炉渣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着原子序数的递增,八种短周期元素(用字母x、y、z……表示)的原子半径相对大小、最高正价或最低负价的变化如下图所示。

请回答下列问题:
(1)f在周期表中的位置为______________;x形成的阴离子的结构示意图为_____________________。
(2)比较d、e常见离子的半径大小:__________________(填化学式,下同);比较g、h的最高价氧化物对应水化物的酸性强弱:_______________________。
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶2∶1 ∶4,其化学式为__________________________。
②能形成共价化合物,写出其中一种的结构简式____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是从我国特产植物中提取的一种生物碱,其人工合成路线如图:
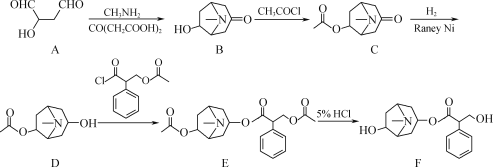
(1)A中含氧官能团的名称为___和___。
(2)C→D的反应类型为___。
(3)E→F的过程中,会有副产物X(分子式为C8H15NO2)生成,写出X的结构简式:___。
(4)C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:__。
①分子中有醚键;
②能与FeCl3溶液发生显色反应,能与盐酸反应;
③有4种不同化学环境的氢且数目比为9∶2∶2∶2。
(5)已知:R—O—R′+2HBr![]() R—Br+R′—Br十H2O(R、R′表示烃基)。
R—Br+R′—Br十H2O(R、R′表示烃基)。
写出以![]() 、CH3NH2和CO(CH2COOH)2为原料制备
、CH3NH2和CO(CH2COOH)2为原料制备![]() 的合成路线流程图___(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图___(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷精矿湿法制备磷酸的一种工艺流程如下:

已知:磷精矿主要成分:Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。
(1)上述流程中所采取的实验措施能加快反应速率有_____________。
(2)酸浸时,磷精矿中Ca5(PO4)3(OH)与H2SO4反应的化学方程式为_____________。
(3)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因______。
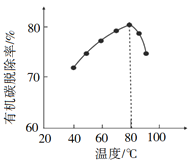
(4)脱硫时,CaCO3稍过量,充分反应后仍有SO42-残留,加入BaCO3代替CaCO3可进一步提高硫的脱除率,原因是_____。向粗磷酸中加入BaCO3脱硫,发生反应的离子方程式是_____。
(5)取ag所得精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用b mol·L-1 NaOH 溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液c L,精制磷酸中H3PO4的质量分数是_____。(已知摩尔质量为98g·mol-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)、如图为一“铁链”图案,小明在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:
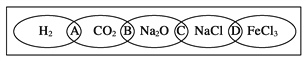
(1)请将分类依据代号填入相应的括号内:
(______)两种物质都不是电解质
(______)两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的图中某种物质M的溶液加热至呈红褐色。
①物质M的化学式为________________。
②证明有红褐色胶体生成的实验操作是________________________________________。
(Ⅱ)反应:A.2F2+2H2O=4HF+O2↑; B.2Na+2H2O=2NaOH+H2↑;
C.CaO+H2O=Ca(OH)2; D.2H2O=2H2↑+O2↑。
其中水是氧化剂的是______,水是还原剂的是________。(填序号)
(Ⅲ)反应:3Cu + 8HNO3 = 3Cu(NO3)2+2NO↑+4H2O,还原剂与氧化剂的物质的量之比:_______,当有0.6mol电子转移时。生成的NO在标准状况的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、钴、硼、镓、硒等。回答下列问题:
(1)基态二价铜离子的电子排布式为______,已知高温下Cu2O比CuO更稳定,试从核外电子排布角度解释______。
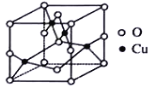
(2)铜的某种氧化物晶胞如图,该晶胞中阴离子的个数为_________。
(3)铜与(SCN)2反应生成Cu(SCN)2,中心体为___________,HSCN结构有两种,硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的原因是_________。
(4)BF3能与NH3反应生成BF3·NH3。B与N之间形成配位键,氮原子提供_____,第二周期元素中,电离能介于B和N之间的元素有_______个。
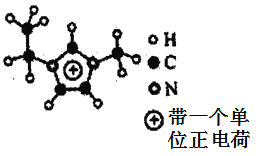
(5)如图EMIM+离子中,碳原子的杂化方式是___________。分子中的大π键可用符号πnm表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为π66),则EMM+离子中的大π键应表示为___________。
(6)如图六方氮化硼晶体结构与石墨晶体相似,则六方氮化硼晶体中层间的相互作用为___________。六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构、硬度与金刚石相似,其晶胞如图,晶胞边长为361.5pm,立方氮化硼的密度是___________g·cm-3(只列算式,![]() 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一绝热(不与外界发生热交换)的恒容容器中,发生反应:2A(g)+B(s) ![]() C(g)+D(g),下列描述中不能表明反应已达到平衡状态的是( )
C(g)+D(g),下列描述中不能表明反应已达到平衡状态的是( )
A. 混合气体的密度不变 B. 单位时间内生成n molD,同时生成n molC
C. 混合气体的平均相对分子质量不变 D. C(g)的物质的量浓度不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com