
����Ŀ���������ȽϹ��������ڲ�ͬ�����µķֽ���ʵ���������ݣ���ش�
��� | ������� | �������� | ʵ������ | |
1 | 2mL | H2O2��Һ+2����ˮ | ���� | ������ |
2 | 2mL | H2O2��Һ+2����ˮ | 90��ˮԡ | �������ݣ������ǵ������㲻��ȼ |
3 | 2mL | H2O2��Һ+2����������Ϊ3.5%FeCl3��Һ | ���� | �϶����ݣ������ǵ������㸴ȼ |
4 | 2mL | H2O2��Һ+2�θ�����ĥҺ | ���� | �������ݣ������ǵ����������Ҹ�ȼ |
��1����ʵ���У�ʵ������ �����Թܱ�ţ����Ա����� ���������ø�Ĵ����ԣ�
��2���Ƚ�1 �ź�2 ���Թܣ���ó��Ľ����� ���Ƚ�3�ź�4���Թܣ���ó��Ľ����� ��
��3��ijͬѧ���ձ��з����������ʵ�飬����Թ�3��ʵ��4������պ��෴������Ϊʵ��ʧ�ܵ�ԭ��������ǣ� ��
��4�����ͼ��ʾ�¶ȶ�ø�Ĵ�Ч�ʵ�Ӱ�죬���ͼ�ش������е�AB �α������¶ȵ���40��ʱ��ø�Ļ������¶����߶���ǿ���������е�BC �α��� ��

���𰸡���1��2��3��4 �¶Ⱥͼ����Լ��ȷ�Ӧ����
��2����������߹�������ֽⷴӦ�����ʹ�������ø��Fe3+�Ĵ�Ч�ʸߵö�
��3��������ĥҺ������
��4�����¶ȸ���40��ʱ��ø�Ļ������¶����߶��½�
�������������������1����ʵ���У���һ���ǹ�����������Ȼ����������ֽ⣬�ǿհ����飬2��3��4��ֱ����¶�90�ȡ��μ��Ȼ�����Һ���μӸ�����ĥҺ�Թ�������ֽ����ʵ�Ӱ��
��ʵ������2��3��4���Ա������¶Ⱥͼ����Լ��ȷ�Ӧ������
��2��1 �ź�2 ���Թܵı������¶ȣ��Ƚ�1 �ź�2 ���Թܣ��ó��Ľ����Ǽ�������߹�������ֽⷴӦ�����ʣ�3�ź�4���Թܵı��������ӵĴ��������ͬ���Ƚ�3�ź�4���Թܣ��ó��Ľ����ǣ���������ø��Fe3+�Ĵ�Ч�ʸߵö࣮
��3��ijͬѧ���ձ��з����������ʵ�飬����Թ�3��ʵ��4������պ��෴�����ܵ�ԭ���ǣ�������ĥҺ�����ʣ���������ø������ֽ⣮
��4��B���������¶ȣ�ø�Ĵ�Ч��������¶ȸ���40��ʱ������BC�¶ȷ�Χ�ڣ����¶����ߣ�ø�Ĵ�Ч�ʽ��ͣ�
�ʴ�Ϊ����1��2��3��4 �¶Ⱥͼ����Լ��ȷ�Ӧ����
��2����������߹�������ֽⷴӦ�����ʹ�������ø��Fe3+�Ĵ�Ч�ʸߵö�
��3��������ĥҺ������
��4�����¶ȸ���40��ʱ��ø�Ļ������¶����߶��½�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������������ʵ������������±���ʾ:
�ɷ� | SiO2 | MgO | Fe2O3 | Al2O3 | CuO |
��������/% | ? | 4.0 | 32 | 10.2 | 16 |
��֪�����£������������↑ʼ��������ȫ������pH���±���ʾ:
Cu(OH)2 | Mg(OH)2 | Fe(OH)3 | Al(OH)3 | |
��ʼ������pH | 4.8 | 9.3 | 2.7 | 3.8 |
��ȫ������pH | 6.4 | 10.8 | 3.7 | 4.7 |
ij������������������Ϊԭ���Ʊ�����������ͭ�������䲿�ֹ����������£�
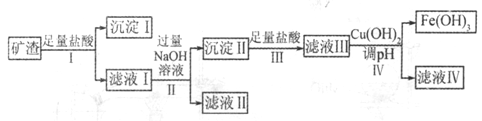
��ش��������⣺
��1������I����Ҫ��;��_______(��һ�����ɣ�������IV�е���pH��ΧΪ______��
��2������ҺII��������Ӧ�ɵõ���Ҫ�Ʊ���һ�ֽ������������ҺII����Ҫͨ������Ļ�ѧʽΪ__________��
��3��д������ҺI�õ���ҺII�����ӷ���ʽ:______________��
��4����ҺIV�к��еĽ�����������__________��������������ӵIJ�����____________��
��5����ҵ�ϣ�ұ����������ͭ��þ�ķ���������_______(����ĸ����
A.��ⷨ���Ȼ�ԭ�����ֽⷨ���ֽⷨ
B.��ⷨ���Ȼ�ԭ�����Ȼ�ԭ������ⷨ
C.�Ȼ�ԭ�����ֽⷨ����ⷨ����ⷨ .
D.�Ȼ�ԭ�����Ȼ�ԭ�����Ȼ�ԭ������ⷨ
��6����ҵ��ұ����������ͭ��þʱѡ�õ���Ӧ��ԭ��Ϊ___________(����ĸ����
A.Al2O3��Fe2O3��CuO��MgO
B.Al2O3��Fe2O3��CuCl2��MgCl2
C.AlCl3��FeCl3��CuO��MgCl2
D. Al2O3��Fe2O3��CuO��MgCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪X(g)��Y(g)�����ת����2X(g)![]() Y(g) ��H<0���ֽ�һ����X(g)��Y(g)�Ļ������ͨ��һ���Ϊ1 L�ĺ����ܱ������У���Ӧ�P�������Ũ����ʱ��仯�Ĺ�ϵ��ͼ��ʾ��������˵������ȷ����
Y(g) ��H<0���ֽ�һ����X(g)��Y(g)�Ļ������ͨ��һ���Ϊ1 L�ĺ����ܱ������У���Ӧ�P�������Ũ����ʱ��仯�Ĺ�ϵ��ͼ��ʾ��������˵������ȷ����

A������������ѹǿ���䣬��˵����Ӧ�Ѵﻯѧƽ��״̬
B��a��b��c��d�ĸ����ʾ�ķ�Ӧ��ϵ�У���ʾ��ѧ��Ӧ����ƽ��״̬��ֻ��b��
C��25��30 min����X��ʾ��ƽ����ѧ��Ӧ������0.08 mol��L��1��min��1
D����Ӧ������25 minʱ�����߷����仯��ԭ��������Y��Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1 mol CO��2 mol H2����һ�ݻ�Ϊ1L���ܱ����������ֱ���250��C��T��C�·��� ��Ӧ:CO(g)+2H2(g)��CH3OH(g)����H=a kJ/mol,��ͼ�����з�������ȷ����

A��250��Cʱ��010minH2 ��Ӧ����Ϊ 0.015 mol,/(L.min)
B��ƽ��ʱCO��ת������T��ʱС��250��ʱ
C��������������������С�ݻ������CO�����������
D��a<0,ƽ�ⳣ��K:T0Cʱ����2500C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3��2 L���ܱ�������������ͬ���¶��¡�ʹ����ͬ�Ĵ����ֱ���з�Ӧ��N2(g)+3H2(g)![]() 2NH3(g)������ͬ��ʽͶ�뷴Ӧ�������ֺ��¡���������÷�Ӧ�ﵽƽ��ʱ�й�����������
2NH3(g)������ͬ��ʽͶ�뷴Ӧ�������ֺ��¡���������÷�Ӧ�ﵽƽ��ʱ�й�����������
���� | �� | �� | �� |
��Ӧ���Ͷ���� | 3 mol H2�� 2 mol N2 | 6 mol H2�� 4 mol N2 | 2 mol NH3 |
�ﵽƽ���ʱ��/min | 5 | 8 | |
ƽ��ʱN2��Ũ��/(mol��L1) | c1 | 1.5 | |
NH3��������� | ��1 | ��2 | |
���������ܶ�/(g��L1) | ��1 | ��2 |
����˵������ȷ����
A���������з�Ӧ�ӿ�ʼ����ƽ��ķ�Ӧ����Ϊv(H2)=0.3 mol��L1��min1
B���ڸ��¶��¼������з�Ӧ��ƽ�ⳣ��K=![]()
C��2��1=��2
D��2c1<1.5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����������
A. ����ԭ�Ӱ뾶��С��Ԫ�� B. ���Ƿǽ�������ǿ��Ԫ��
C. ��Ԫ���ʺ����뵼����� D. ϡ������Ԫ��ԭ�ӵ�������������Ϊ8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������X������Y��0.16 mol����10 L�����ܱ������У�������ӦX(g)��Y(g)![]() 2Z(g) ��H<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g) ��H<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ����
A����Ӧǰ2 min��ƽ������v(Z)��2.0��10��3 mol/(L��min)
B�������������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰv(��)>v(��)
C�����¶��´˷�Ӧ��ƽ�ⳣ��K��1.44
D�������������䣬�ٳ���0.2 mol Z��ƽ��ʱX�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������а�Ĥ�������¶�Ϊ45��������ø�������¶�Ϊ37������Һ����ø������������Ϊ5%����ѿ����Һ��������Һ��������Һ�����ɡ�ij����С���Ա����������ʵ����ϼ���ͼʵ��װ�ý�������֤ø����רһ������ʵ�顣


ʵ�鲽�����£�
��ش��������⣺
��1����������Ϊ��ʹU�ιܵ�A��B���˳�ʼҺ��ƽ�룬B��Ӧ�ü���_______����ʱ��Ĥ��_______��������������������������������ԭ����_______��
��2��������Ӧ�ÿ��Ƶ��¶�Ϊ_______�����������е�ij��øΪ____��
��3����Բ������е�ʵ�������������Ľ��ͣ�____��
��4���������У��ʵ�ʱ������ֱ�ȡU�ι�A��B�˵���Һ����������Լ�����ˮԡ���ȣ���ʵ��������______���ý��_______������������������������֤ø����רһ�ԡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����백ˮ��Ӧ����������� ( )
A. ������Һ B. ���� C. �������� D. ����ͭ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com