
| A.Cu、Fe3+ | B.Fe2+、Fe3+ | C.Cu、Cu2+ | D.Cu、Fe2+ |
科目:高中化学 来源:不详 题型:单选题
| A.分别还原a mol Fe2O3所需H2、Al、CO物质的量之比为3 ∶2 ∶3 |
| B.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4 |
| C.工业上可用铁制容器储存、运输浓硝酸、浓硫酸 |
| D.检验某物质是否含Fe2O3的操作步骤为:样品→粉碎→加热→溶解→过滤→向滤液中加KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | | Fe2+具有还原性 |
| ② | 在FeCl2溶液中加入锌片 |  | Zn+Fe2+=Zn2++Fe | |
| ③ | 在FeCl3溶液中加入足量铁粉 | | Fe+2Fe3+=3 Fe2+ | Fe3+具有氧化性 |
| ④ | |  | | Fe3+具有氧化性 |
| A.Cl2 | B.Na | C.Na+ | D.Cl- E.SO2 F.NO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

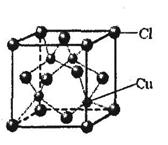
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.所加入硝酸的浓度是4 mol/L |
| B.加入硝酸10 mL时,剩余金属为铁和铜 |
| C.共加入硝酸20 mL时,剩余金属只有铜 |
| D.如果在金属混合物中共加入硝酸40 mL时,生成的NO仍是0.672 L(标准状况) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属/g | 18.0 | 9.6 | 0 | 0 |
| NO体积/mL | 2240 | 4480 | 6720 | V |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com