
| A. | 第一电离能:N>O | B. | 第一电子亲和能:F<Cl | ||
| C. | 电负性:O<Cl | D. | 共价键的键角:NH3<H2S |
分析 A.N的2p电子半满为稳定结构;
B.元素处于基态时的气态原子获得1个电子成为-1价阴离子时所放出的能量叫做该元素的第一电子亲和能,非金属性越强,元素得电子能力越强,其电子亲和能越大;
C.非金属性越强,电负性越大;
D.氨气为三角锥型,NH3分子中共价键键角为107°,H2S分子中共价键键角接近90°,为V型.
解答 解:A.N的2p电子半满为稳定结构,难失去电子,则第一电离能:N>O,故A正确;
B.非金属性越强,元素得电子能力越强,其电子亲和能越大,则第一电子亲和能:F>Cl,故B错误;
C.非金属性越强,电负性越大,则电负性:O>Cl,故C错误;
D.氨气为三角锥型,NH3分子中共价键键角为107°,H2S分子中共价键键角接近90°,为V型,则共价键的键角:NH3>H2S,故D错误;
故选A.
点评 本题考查元素的性质,为高频考点,把握电子排布规律、电负性的比较方法等为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
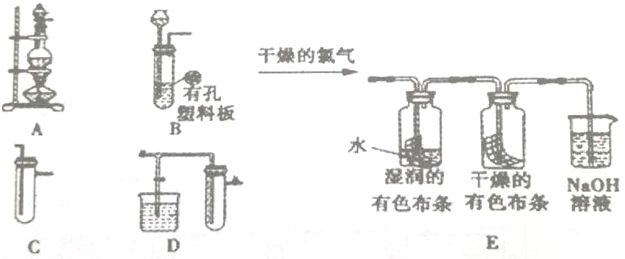
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
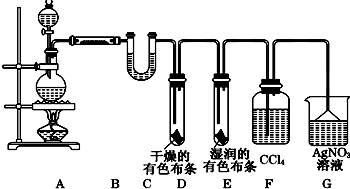
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热晶体时先用小火,后渐改为用大火加热至晶体变白 | |
| B. | 灼烧时如有晶体溅出容器,应再加一些晶体继续加热 | |
| C. | 加热后的冷却放在干燥器中进行 | |
| D. | 加热、冷却、称量,重复多次即是恒重操作 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 时间t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
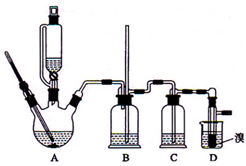 实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中发生如下反应:CH2=CH2+Br2→BrCH2CH2Br.可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题:
实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中发生如下反应:CH2=CH2+Br2→BrCH2CH2Br.可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com