
Éč°¢·ü¼ÓµĀĀŽ³£ŹżĪŖNA£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®1mol Cl2Óė×ćĮæFe·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ3NA
B£®20gÖŲĖ®£ØD2O£©ÖŠŗ¬ÓŠµÄÖŠ×ÓŹżĪŖ8 NA
C£®³£ĪĀ³£Ń¹ĻĀ£¬46gµÄNO2ŗĶN2O4»ģŗĻĘųĢåŗ¬ÓŠµÄŌ×ÓŹżĪŖ3NA
D£®±ź×¼×“æöĻĀ£¬22.4LŅŃĶéÖŠ¹²¼Ū¼üŹżÄæĪŖ19NA
 ½×ĢŻ¼ĘĖćĻµĮŠ“š°ø
½×ĢŻ¼ĘĖćĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ¹ć¶«øßæ¼·šÉ½ŹŠøßČż¶žÄ£Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¹ŲÓŚĻĀĮŠ×°ÖĆĖµ·ØÕżČ·µÄŹĒ

A£®×°ÖĆ¢ŁÖŠµÄĶ°ōÉĻĆ°ĘųÅŻ
B£®Čōa”¢b¼«ŹĒŹÆÄ«£¬×°ÖĆ¢ŚÖŠµÄa”¢b Ć°ĘųÅŻ
C£®×°ÖĆ¢Ł»»ÉĻĮņĖįĶČÜŅŗ£¬½«ŹµĻÖŠæʬÉĻ¶ĘĶ
D£®×°ÖĆ¢Ś»»ÉĻĮņĖįĶČÜŅŗ£¬½«ŹµĻÖ”°b¼«”±¶ĘĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÖŲĒģŹŠøßČżĻĀѧʌ¶žÄ£æ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĶʶĻĢā
(±¾Ģā¹²14·Ö)ijõ„(H)ŹĒŅ»ÖÖŗĻ³É¶ą»·»ÆŗĻĪļµÄÖŠ¼äĢ壬æÉÓÉĻĀĮŠĀ·ĻßŗĻ³É(²æ·Ö·“Ó¦Ģõ¼žĀŌČ„)£ŗ
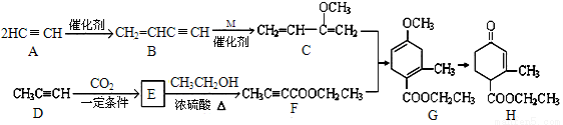
£Ø1£©A”śBµÄ·“Ó¦ĄąŠĶŹĒ £¬B”śCĪŖ¼Ó³É·“Ó¦£¬Ōņ»ÆŗĻĪļMµÄ½į¹¹¼ņŹ½ŹĒ £»
£Ø2£©HÖŠ³żĮĖōŹ»ł(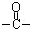 )Ķā£¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĆū³ĘŹĒ £»
)Ķā£¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĆū³ĘŹĒ £»
£Ø3£©ŹµŃéŹŅÖĘAµÄ»Æѧ·½³ĢŹ½ĪŖ £»
£Ø4£©E”ś FµÄ»Æѧ·½³ĢŹ½ŹĒ £»
£Ø5£©ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ”£
a. DŗĶFÖŠ¾łŹōÓŚČ²ĢžĄąĪļÖŹ
b. AÄÜŗĶHCl·“Ó¦µĆµ½¾ŪĀČŅŅĻ©µÄµ„Ģå
c. 1mol GĶźČ«Č¼ÉÕÉś³É7mol H2O
d. HÄÜ·¢Éś¼Ó³É”¢Č”“ś·“Ó¦
£Ø6£©TMOBŹĒHµÄĶ¬·ÖŅģ¹¹Ģ壬¾ßÓŠĻĀĮŠ½į¹¹ĢŲÕ÷£ŗ¢ŁŗĖ“Ź²ÕńĒāĘ×±ķĆ÷£¬·Ö×ÓÖŠ³ż±½»·Ķā£¬ĘäĖüĒāŌ×Ó»Æѧ»·¾³ĻąĶ¬£»¢Ś“ęŌŚ¼×Ńõ»ł(CH3O-)”£TMOBµÄ½į¹¹¼ņŹ½ŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğĢģ½ņŹŠøßČżĖÄŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A£®ŅŃÖŖµēĄėĘ½ŗā³£Źż£ŗH2CO3£¾HClO£¾HCO3”Ŗ£¬ĻņNaClOČÜŅŗÖŠĶØČėÉŁĮæCO2£ŗ2ClO”Ŗ+CO2+H2O£½2HClO+CO32”Ŗ
B£®ĻņĮņĖįĒāÄĘČÜŅŗÖŠµĪ¼ÓBa(OH)2ÖĮÖŠŠŌ£ŗH++SO42-+Ba2++ OH-£½BaSO4”ż+ H2O
C£®Fe(NO3)3ČÜŅŗÖŠ¼ÓČė¹żĮæµÄHIČÜŅŗ£ŗ2Fe3£« + 2I££½2Fe2£« + I2
D£®ĮņĒāøłĄė×ӵĵēĄė·½³ĢŹ½£ŗHS££«H2O H3O£«£«S2£[
H3O£«£«S2£[
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÉĀĪ÷Ź”Ī÷°²ŹŠøßČżĻĀѧʌŅ»Ä£Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®t”ꏱ£¬Ä³ČÜŅŗµÄpH£½6£¬ŌņøĆČÜŅŗŅ»¶ØĪŖĖįŠŌ
B£®³£ĪĀĻĀ£¬½«pH£½11µÄ°±Ė®Ļ”ŹĶŗó£¬ČÜŅŗÖŠĖłÓŠĄė×ÓµÄÅØ¶Č¾ł½µµĶ
C£®³£ĪĀĻĀ£¬½«pH£½11µÄNaOHČÜŅŗŗĶpH£½3µÄCH3COOHČÜŅŗµČĢå»ż»ģŗĻŗó£¬ČÜŅŗµÄpH£¼7
D£®³£ĪĀĻĀ£¬ĪļÖŹµÄĮæÅضČŗĶĢå»żĻąĶ¬µÄK2CO3”¢K2SO4”¢HC1ČÜŅŗ»ģŗĻŗó£¬ČÜŅŗµÄpH£¼7
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015Ń§ÄźÉ½¶«Ź¦“óø½ÖŠøßČżµŚĘß“ĪÄ£Äāæ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
£Ø19·Ö£©Ä³æĪĶāŠ”×é¶ŌŅ»Š©½šŹōµ„ÖŹŗĶ»ÆŗĻĪļµÄŠŌÖŹ½ųŠŠŃŠ¾æ”£
£Ø1£©ĻĀ±ķĪŖ”°ĀĮÓėĀČ»ÆĶČÜŅŗ·“Ó¦”±ŹµŃé±ØøęµÄŅ»²æ·Ö£ŗ
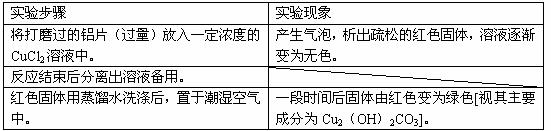
°“·“Ó¦ĄąŠĶŠ“³öŹµŃéÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ø÷Ņ»øö£ØŹĒĄė×Ó·“Ó¦µÄÖ»Š“Ąė×Ó·½³ĢŹ½£©
ÖĆ»»·“Ó¦____________________________________________________________£»
»ÆŗĻ·“Ó¦____________________________________________________________”£
£Ø2£©¹¤ŅµÉĻæÉÓĆĀĮÓėČķĆĢæó£ØÖ÷ŅŖ³É·ÖĪŖMnO2£©·“Ó¦Ą“Ņ±Į¶½šŹōĆĢ”£MnO2ŌŚH2O2·Ö½ā·“Ó¦ÖŠ×÷“߻ƼĮ”£Čō½«ŹŹĮæMnO2¼ÓČėĖį»ÆŗóµÄH2O2ČÜŅŗÖŠ£¬MnO2Čܽā²śÉśMn2+”£øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ ”£
£Ø3£©Ä³æĪĶāŃŠ¾æŠ”×飬ÓĆŗ¬ÓŠ½Ļ¶ąŌÓÖŹµÄĶ·Ū£¬Ķعż²»Ķ¬µÄ»Æѧ·“Ó¦ÖĘČ”µØ·Æ”£ĘäÉč¼ĘµÄŹµŃé¹ż³ĢĪŖ£ŗ
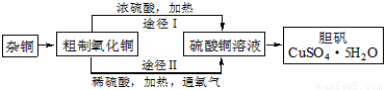
¢ŁĶÖŠŗ¬ÓŠ“óĮæµÄÓŠ»śĪļ£¬æɲÉÓĆ×ĘÉյķ½·Ø³żČ„ÓŠ»śĪļ£¬×ĘÉÕŹ±½«“ÉŪįŪöÖĆÓŚ ÉĻ£ØÓĆŅŌĻĀĖłøųŅĒĘ÷µÄ±ąŗÅĢīČė£¬ĻĀĶ¬£©£¬Č”ÓĆŪįŪöÓ¦Ź¹ÓĆ £¬×ĘÉÕŗóµÄŪįŪöÓ¦·ÅŌŚ ÉĻ£¬²»ÄÜÖ±½Ó·ÅŌŚ×ĄĆęÉĻ”£
ŹµŃéĖłÓĆŅĒĘ÷£ŗ
a Õō·¢Ćó
b ŹÆĆŽĶų
c Ĺȿ½Ē
d ±ķĆęĆó
e ŪįŪöĒÆ
f ŹŌ¹Ü¼Š
¢ŚÓÉ“ÖÖĘŃõ»ÆĶĶعżĮ½ÖÖĶ¾¾¶ÖĘČ”µØ·Æ£¬ĶعżĶ¾¾¶¢ņŹµĻÖÓĆ“ÖÖĘŃõ»ÆĶÖĘČ”µØ·Æ£¬±ŲŠė½ųŠŠµÄŹµŃé²Ł×÷²½Öč£ŗĖįČÜ”¢¼ÓČČĶØŃõĘų”¢¹żĀĖ”¢ ”¢ĄäČ“½į¾§”¢ ”¢×ŌČ»øÉŌļ£¬ÓėĶ¾¾¶¢ńĻą±Č£¬Ķ¾¾¶¢ņÓŠĆ÷ĻŌµÄĮ½øöÓŵćŹĒ£ŗ ”¢ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015Ń§ÄźÉ½¶«Ź¦“óø½ÖŠøßČżµŚĘß“ĪÄ£Äāæ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¶ĢÖÜĘŚÖ÷×åŌŖĖŲX”¢Y”¢Z”¢WµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó”£XŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒĘäÄŚ²ćµē×ÓŹżµÄ2±¶£¬YŹĒµŲæĒÖŠŗ¬Įæ×īøßµÄŌŖĖŲ£¬Z2£«ÓėY2£¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹£¬WÓėXĶ¬Ö÷×唣ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®Ąė×Ó°ė¾¶£ŗr(Y2£)£¾r(Z2£«)
B£®Y·Ö±šÓėZ”¢WŠĪ³ÉµÄ»ÆŗĻĪļÖŠ»Æѧ¼üĄąŠĶĻąĶ¬
C£®YµÄĘųĢ¬¼ņµ„Ēā»ÆĪļµÄČČĪČ¶ØŠŌ±ČµŖŌŖĖŲµÄĘųĢ¬¼ņµ„Ēā»ÆĪļČõ
D£®X”¢Y”¢Z”¢WĖłÓŠŌŖĖŲµÄ×īøßÕż¼ŪµČÓŚĘäĖłŌŚ×åµÄ×åŠņŹż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015Ń§ÄźÉ½¶«Ź”øßČż4ŌĀ¹ż³ĢŠŌ¼ģ²āĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ¼ņ“šĢā
(17·Ö)ŌĖÓĆ»Æѧ·“Ó¦ŌĄķŃŠ¾æĢ¼”¢µŖ”¢ĮņŌŖĖŲ¼°Ęä»ÆŗĻĪļÓŠÖŲŅŖŅāŅ唣
£Ø1£©ŅŃÖŖŅ»¶ØĮæµÄCµ„ÖŹÄÜŌŚO2(g)ÖŠČ¼ÉÕ£¬ĘäæÉÄܵIJśĪļ¼°ÄÜĮæ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ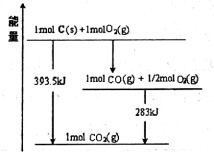
Š“³öCO2(g)ÓėC(s)·“Ӧɜ³ÉCO(g)µÄČČ»Æѧ·½³ĢŹ½_______________________”£
£Ø2£©Ęū³µĪ²Ęų¾»»Æ¹ż³ĢÖŠ·¢Éś·“Ó¦2NO(g)+2CO(g) N2+2CO2(g) ”÷H<0”£Ņ»¶ØĢõ¼žĻĀ£¬ĻņijĆܱÕŗćČŻČŻĘ÷ÖŠ°“Ģå»ż±Č1£ŗl³äČė44.8L(±ź×¼×“æö)NOŗĶCO»ģŗĻĘųĢ壬·¢ÉśÉĻŹö·“Ó¦£¬Ä³Ķ¬Ń§øł¾Ż·“Ó¦¹ż³ĢÖŠµÄÓŠ¹ŲŹż¾Ż»ęÖĘĮĖČēĶ¼ĖłŹ¾ĒśĻß”£
N2+2CO2(g) ”÷H<0”£Ņ»¶ØĢõ¼žĻĀ£¬ĻņijĆܱÕŗćČŻČŻĘ÷ÖŠ°“Ģå»ż±Č1£ŗl³äČė44.8L(±ź×¼×“æö)NOŗĶCO»ģŗĻĘųĢ壬·¢ÉśÉĻŹö·“Ó¦£¬Ä³Ķ¬Ń§øł¾Ż·“Ó¦¹ż³ĢÖŠµÄÓŠ¹ŲŹż¾Ż»ęÖĘĮĖČēĶ¼ĖłŹ¾ĒśĻß”£
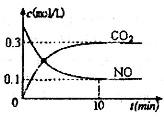
¢ŁĻĀĮŠ¹ŲÓŚÉĻŹö·“Ó¦¹ż³ĢµÄŠšŹöÕżČ·µÄŹĒ ________(ĢīŠ“×ÖÄø“śŗÅ)”£
A£®ĘäĖüĢõ¼ž²»±ä£¬¼ÓČė“߻ƼĮ£¬”÷HµÄÖµ²»±ä
B£®¼°Ź±³żČ„¶žŃõ»ÆĢ¼£¬·“Ó¦µÄÕż·“Ó¦ĖŁĀŹ¼Óæģ
C£®NO”¢CO”¢N2”¢CO2ÅØ¶Č¾ł²»ŌŁ±ä»Æ£¬ĖµĆ÷Ę½ŗāĪ“·¢ÉśŅʶÆ
D£®»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»ŌŁøı䣬֤Ć÷·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬
¢ŚĒ°10minÄŚCOµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ______£¬“ļĘ½ŗāŹ±NOµÄ×Ŗ»ÆĀŹĪŖ_____£¬ÄÜŹ¹ÉĻŹöĘ½ŗāĢåĻµÖŠ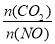 Ōö“óµÄ“ėŹ©ÓŠ__________(ČĪŠ“Ņ»Ģõ)”£
Ōö“óµÄ“ėŹ©ÓŠ__________(ČĪŠ“Ņ»Ģõ)”£
£Ø3£©ŅŃÖŖČõµē½āÖŹŌŚĖ®ÖŠµÄµēĄėĘ½ŗā³£Źż(25”ę)ČēĻĀ±ķ(µ„Ī»Ź”ĀŌ)£ŗ
Čõµē½āÖŹ | H2CO3 | H2SO3 | NH3”¤H2O |
µēĄėĘ½ŗā³£Źż | Ka1=4.2”Į10£7 Ka2=5.6”Į10£11 | Ka1=1.54”Į10£2 Ka2=1.02”Į10£7 | Kb=1.7”Į10£5 |
¢ŁŹŅĪĀĢõ¼žĻĀ”£ÓĆ³ØæŚČŻĘ÷¼ÓČČ°±Ė®Ņ»¶ĪŹ±¼ä£¬»Öø“ÖĮŹŅĪĀŗó£¬ČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č±Č¼ÓČČĒ°_______(ĢīŠ“”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±)ĮĖ£®
¢Ś³£ĪĀĻĀ£¬0.1 mo1”¤L-1(NH4)2SO4ČÜŅŗ³Ź_____(Ģī”°Ėį”±”¢”°ÖŠ”±”¢”°¼ī”±)ŠŌ”£
¢Ū³£ĪĀĻĀ£¬²āµĆijĢ¼ĖįŅūĮĻµÄpH=6£¬ŌņøĆŅūĮĻ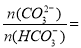 ________”£
________ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗžÄĻŹ”³¤É³ŹŠøßČż5ŌĀŅ»Ä£»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ńó¼»ĖŲŹĒŅ»ÖÖŠĀ½į¹¹ĄąŠĶµÄæ¹ŅŅŠĶøĪŃײ”¶¾ŗĶæ¹°¬×Ģ²”²”¶¾µÄ»ÆŗĻĪļ£¬Ęä½į¹¹ČēĶ¼ĖłŹ¾£¬ÓŠ¹ŲŃó¼»ĖŲµÄĖµ·ØÕżČ·µÄŹĒ
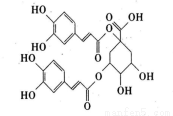
A£®Ńó¼»ĖŲµÄ»ÆѧŹ½ĪŖC25H22O12
B£®”Ŗ¶ØĢõ¼žĻĀÄÜ·¢Éśõ„»ÆŗĶĻūČ„·“Ó¦
C£®1molŃó¼»ĖŲ×īÉŁæÉÓŠ14molŌ×Ó¹²Ę½Ćę
D£®1 molŃó¼»ĖŲ×ī¶ąæÉĻūŗÄ9mol NaOHŗĶ6mol Br2
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com