
| A. | 减小H2O2溶液的浓度 | B. | 降低温度 | ||
| C. | 加入少量MnO2粉末 | D. | 向溶液中加入蒸馏水 |
分析 常见增大反应速率的因素有增大浓度、升高温度、增大压强、加入催化剂以及增大固体的表面加等,以此解答该题.
解答 解:A.减小H2O2溶液的浓度,单位体积活化分子数目减小,则反应速率减小,故A错误;
B.降低H2O2溶液的温度,活化分子百分数减小,则反应速率减小,故B错误;
C.向H2O2溶液中加入少量MnO2粉末,二氧化锰起到反应的催化剂的作用,可增大反应速率,故C正确;
D.加入少量蒸馏水,浓度减小,反应速率减小,故D错误.
故选C.
点评 本题考查化学反应速率的影响以及化学平衡状态的判断等问题,为高考常见题型和高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阿司匹林课解热镇痛,常用于治疗感冒 | |
| B. | 氢氧化钠能中和胃酸,可用于治疗胃酸过多 | |
| C. | 蚕丝的主要成分是纤维素 | |
| D. | 合金中一定只含金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
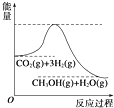 (1)盖斯定律的含义是:对于一个化学反应,无论是一步完成还是分几步完成,其反应焓变都是相同的,换句话说:化学反应的反应热只与体系的始态和终态有关,而与反应的途径无关
(1)盖斯定律的含义是:对于一个化学反应,无论是一步完成还是分几步完成,其反应焓变都是相同的,换句话说:化学反应的反应热只与体系的始态和终态有关,而与反应的途径无关查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56 | B. | 56 g•mol-1 | C. | 28 | D. | 28 g•mol -1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com