
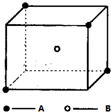
 某离子晶体晶胞结构如图所示,A位于立方体的顶点,B位于立方体中心.试分析:
某离子晶体晶胞结构如图所示,A位于立方体的顶点,B位于立方体中心.试分析:分析 由离子晶体晶胞图,A位于立方体的顶点,B位于立方体中心,则1个晶胞中含A为4×$\frac{1}{8}$=$\frac{1}{2}$,含B为1,A、B的离子个数之比为1:2,1个B与4个A形成空间正四面体结构,以此来解答.
解答 解:(1)由离子晶体晶胞图,A位于立方体的顶点,B位于立方体中心,则每个B同时吸引着4个A,空间有8个晶胞无隙并置,则每个A同时吸引着8个B,1个晶胞中含A为4×$\frac{1}{8}$=$\frac{1}{2}$,含B为1,A、B的离子个数之比为1:2,则晶体的化学式为XY2或Y2X,
故答案为:4;8;AB2或B2A;
(2)由图可知,A在顶点,则一个晶胞中最近的A有3个,为面上的距离,晶体中在每个A周围与它最接近且距离相等的A共有$\frac{3×8}{2}$=12个,
故答案为:12;
(3)1个B与4个A形成空间正四面体结构,则晶体中距离最近的2个A与1个B形成的夹角∠ABA的度数为109°28′,
故答案为:109°28′.
点评 本题考查晶胞计算,注意X、Y的位置及均摊法计算是解答本题的关键,学生需具有一定的空间想象能力,题目难度中等


科目:高中化学 来源: 题型:选择题
| A. | 111 | B. | 272 | C. | 2007 | D. | 161 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH碱性比KOH强 | |
| B. | Li是最活泼的金属,F是最活泼的非金属 | |
| C. | X2+核外电子数目为18,则X在第四周期第ⅡA族 | |
| D. | 元素周期表有7个副族,7个主族,1个0族,1个Ⅷ族,共16个纵行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
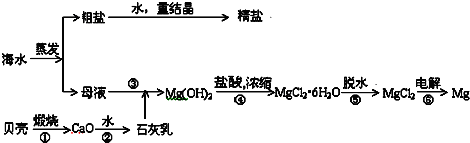
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 | |
| B. | 把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 | |
| C. | 马口铁(镀锡铁)破损时与电解质溶液接触,铁先被腐蚀 | |
| D. | 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com