
在南方人们的主食是大米,在进食时,我们将米饭在嘴中长时间嚼为什么感觉到有甜味呢
A.淀粉在唾液淀粉酶的作用下转变成麦芽糖
B.淀粉中含有葡萄糖
C.淀粉在唾液淀粉酶的作用下转变成葡萄糖
D.淀粉是糖类物质有甜味
科目:高中化学 来源:2014-2015湖南省等三校高一12月联考化学试卷(解析版) 题型:填空题
(13分)过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。回答下列有关双氧水的一些问题:
(1)下述反应中,H2O2仅体现氧化性的反应是(填代号)_________。
A.Na2O2+2HCl == 2NaCl+H2O2
B.Ag2O+H2O2== 2Ag+O2↑+H2O
C.2H2O2 == 2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH == 2K2CrO4+3K2SO4+8H2O
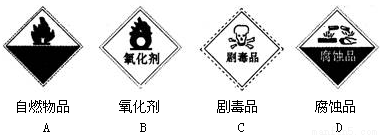
(2)保存过氧化氢的试剂瓶上最适合贴上的一个标签是_________(填字母代号)。
(3)某强酸性反应体系中,反应物和生成物共六种物质或离子:O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2↑。
①写出该反应的离子方程式并配平___________________________________________。
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子数目为_________。
(4)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+ H2O2+ H2O==A+NH3↑,试指出生成物A的化学式为__________________,并阐明H2O2被称为“绿色氧化剂”的理由是_____________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列表达中不正确的是
A.1molH2 B.2molNa2CO3 C.2molOH D.0.5mol氧
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省高二上学期期中化学(文)试卷(解析版) 题型:选择题
2016年我国将实施新的《环境空气质量标准》.下列措施有利于改善大气质量、保护环境的是
A.大力发展火力发电
B.加高工厂的烟囱,使烟尘和废气远离地表
C.开发利用太阳能、氢能等新能源
D.焚烧城市垃圾不露天堆放
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省高二上学期期中化学(文)试卷(解析版) 题型:选择题
改革开放以来,祖国越来越富强,人民生活水平不断提高,不合理的饮食习惯严重影响身体健康,下列饮食习惯科学的是
A.多吃肉,少吃蔬菜水果
B.合理摄入糖类、油脂等,注意膳食平衡
C.为防止变胖,炒菜时不放油
D.多饮用纯净水,少饮用矿泉水
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省高二上学期期中化学(文)试卷(解析版) 题型:选择题
人体生命活动需要微量元素的参与,贫血是缺少下列哪种微量元素
A.碘 B.锌 C.铁 D.铜
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高二上学期第三次月考化学试卷(解析版) 题型:选择题
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中正确的是
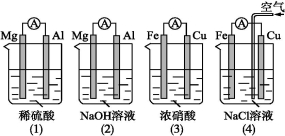
A.(1)(2)中Mg作负极,(3)(4)中Fe作负极
B.(2)中Mg作正极,电极反应式为6H2O+6e- 6OH-+3H2↑
6OH-+3H2↑
C.(3)中Fe作负极,电极反应式为Fe-2e- Fe2+
Fe2+
D.(4)中Cu作正极,电极反应式为2H++2e- H2↑
H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期第四次月考化学试卷(解析版) 题型:填空题
选做[有机化学]](10分)邻羟基桂皮酸(IV)是合成香精的重要原料,下列为合成邻羟基桂皮酸(IV)的路线之一
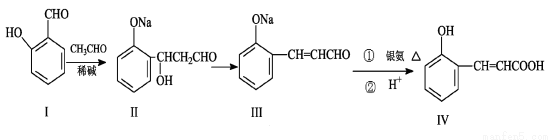
试回答:
(1)I中含氧官能团的名称 和 。
(2)II→III的反应类型 。
(3)① IV与乙醇和浓硫酸混合加热的化学方程式 。
② IV与过量NaOH溶液反应的化学方程式 。
(4)有机物X与IV互为同分异构体,且X有如下特点:
① 是苯的对位取代物, ② 能与NaHCO3反应放出气体 ,③能发生银镜反应。
请写出X的一种结构简式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期10月月考化学试卷(解析版) 题型:填空题
(12分)甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g) + 2H2(g)  CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ:CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
①下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
②某温度下,将2mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 (从上表中选择)。
(2)已知在常温常压下:
①2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(l) ΔH1=-1451.6kJ/mol
②2CO (g)+ O2(g) = 2CO2(g) ΔH2 =-566.0kJ/mol
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置:

①工作一段时间后,测得溶液的pH减小。请写出该电池的负极的电极反应式。
②用该电池电解(惰性电极)500mL某CuSO4溶液,电解一段时间后,为使电解质溶液恢复到原状态,需要向溶液中加入9.8g Cu(OH)2固体。则原CuSO4溶液的物质的量浓度为 mol/L(假设电解前后溶液体积不变)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com