
【题目】室温下,现有A、B、C、D、E、F六种常见化合物,已知它们的阳离子有K+、Ag+、Ca2+、Ba2+、Fe2+、Al3+ , 阴离子有Cl﹣、OH﹣、CH3COO﹣、NO3﹣、SO42﹣、CO32﹣ , 现将它们分别配成0.1mol/L的溶液,进行如下实验:(已知:室温下,饱和氢氧化钙溶液浓度约为0.00165 g/mL)
①测得溶液A、C、E呈碱性,且碱性为A>E>C;
②向B溶液中滴加Na2S溶液,出现难溶于强酸且阴阳离子个数比为1:2的黑色沉淀;
③向D溶液中滴加Ba(NO3)2溶液,无明显现象;
④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色.
根据上述实验现象,回答下列问题:
(1)写出下列化合物的化学式:A、B、C .
(2)实验④中白色沉淀变为红褐色对应的化学方程式:
(3)D与E的溶液反应离子方程式是: .
【答案】
(1)Ba(OH)2;AgNO3;Ca(CH3COO)2
(2)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(3)2Al3++3CO ![]() +3H2O=2Al(OH)3↓+3CO2↑
+3H2O=2Al(OH)3↓+3CO2↑
【解析】解:已知:室温下,饱和氢氧化钙溶液浓度约为0.00165 g/mL,则1L溶液中最多含有1.65g钙离子,最大物质的量为: ![]() =0.04125mol,即:氢氧化钙的最大浓度小于0.04125mol/L,则六种化合物中不可能含有氢氧化钙,①测得溶液A、C、E呈碱性,三种溶液为碱液或水解呈碱性的溶液,且碱性为A>E>C,则A为碱,溶液中含有大量的OH﹣离子,OH﹣离子与Ag+ , Ca2+ , Fe2+ , Al3+等离子不能大量共存,故A只能为Ba(OH)2 , 根据越弱越水解,E应为碳酸盐,根据离子共存,只能为K2CO3 , C为醋酸盐;②向B溶液中滴加Na2S溶液,出现难溶于强酸且阴阳离子个数比为1:2的黑色沉淀,该黑色沉淀为硫化银,则B为硝酸银溶液;③向D溶液中滴加Ba(NO3)2溶液,无明显现象,说明B中不含SO42﹣离子;④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色,说明F中含有Fe2+离子,综上分析可知,A为Ba(OH)2 , B为AgNO3 , C为Ca(CH3COO)2 , D为AlCl3 , E为K2CO3 , F为FeSO4 , (1)根据分析可知,A为Ba(OH)2 , B为AgNO3 , C为Ca(CH3COO)2 , 所以答案是:Ba(OH)2;AgNO3;Ca(CH3COO)2;(2)氢氧化亚铁在溶液中被氧气氧化成氢氧化铁,反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 , 所以答案是:4Fe(OH)2+O2+2H2O=4Fe(OH)3;(3)D为AlCl3 , E为K2CO3 , 二者混合后发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,反应的离子方程式为:2Al3++3CO
=0.04125mol,即:氢氧化钙的最大浓度小于0.04125mol/L,则六种化合物中不可能含有氢氧化钙,①测得溶液A、C、E呈碱性,三种溶液为碱液或水解呈碱性的溶液,且碱性为A>E>C,则A为碱,溶液中含有大量的OH﹣离子,OH﹣离子与Ag+ , Ca2+ , Fe2+ , Al3+等离子不能大量共存,故A只能为Ba(OH)2 , 根据越弱越水解,E应为碳酸盐,根据离子共存,只能为K2CO3 , C为醋酸盐;②向B溶液中滴加Na2S溶液,出现难溶于强酸且阴阳离子个数比为1:2的黑色沉淀,该黑色沉淀为硫化银,则B为硝酸银溶液;③向D溶液中滴加Ba(NO3)2溶液,无明显现象,说明B中不含SO42﹣离子;④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色,说明F中含有Fe2+离子,综上分析可知,A为Ba(OH)2 , B为AgNO3 , C为Ca(CH3COO)2 , D为AlCl3 , E为K2CO3 , F为FeSO4 , (1)根据分析可知,A为Ba(OH)2 , B为AgNO3 , C为Ca(CH3COO)2 , 所以答案是:Ba(OH)2;AgNO3;Ca(CH3COO)2;(2)氢氧化亚铁在溶液中被氧气氧化成氢氧化铁,反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 , 所以答案是:4Fe(OH)2+O2+2H2O=4Fe(OH)3;(3)D为AlCl3 , E为K2CO3 , 二者混合后发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,反应的离子方程式为:2Al3++3CO ![]() +3H2O=2Al(OH)3↓+3CO2↑, 所以答案是:2Al3++3CO
+3H2O=2Al(OH)3↓+3CO2↑, 所以答案是:2Al3++3CO ![]() +3H2O=2Al(OH)3↓+3CO2↑.
+3H2O=2Al(OH)3↓+3CO2↑.


科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料,某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下三种实验方案。
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。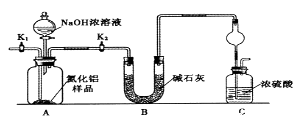
(1)如图C装置中球形干燥管的作用是。
(2)完成以下实验步骤:组装好实验装置,首先;再加入实验药品。接下来的实验操作是,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1 , 通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见。
(4)【方案2】用如下图装置测定m g样品中AlN的纯度(部分夹持装置已略去)。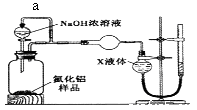
导管a的主要作用是。
(5)为测定生成气体的体积,量气装置中的X液体可以是____________。(填选项序号)
A.CCl4
B.H2O
C.NH4Cl溶液
D.![]()
(6)若m g样品完全反应,测得生成气体的体积为VmL,(已转换为标准状况),则AlN的质量分数为(用含V、m的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于溶液中离子的说法不正确的是( )
A.0.1mol?L﹣1的Na2CO3溶液中粒子浓度关系:c(Na+)═2c(CO ![]() )+2c(HCO
)+2c(HCO ![]() )+2c(H2CO3)
)+2c(H2CO3)
B.常温下,氢氧化钠溶液中滴入醋酸使溶液的pH=7,则混合溶液中醋酸已过量
C.0.2mol?L﹣1的HCl和0.1 mol?L﹣1的NH3?H2O等体积混合后溶液中的离子浓度关系:c(Cl﹣)>c (NH ![]() )>c(H+)>c (OH﹣)
)>c(H+)>c (OH﹣)
D.0.1mol?L﹣1的NaHS溶液中离子浓度关系:c(S2﹣)+c(OH﹣)═c(H+)+c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.用100mL量筒量取1.3mL盐酸
B.配制氯化钠溶液时,用托盘天平称取8.55g氯化钠固体
C.容量瓶不能用作溶解物质的容器
D.粗盐的提纯试验中,滤液在坩埚中加热蒸发结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定体积CO2气体通入到一定浓度的NaOH溶液中,向反应后溶液中滴加相关试剂,下列结论正确的是:( )
A. 逐滴滴加盐酸溶液,立即产生气泡,则生成物只含有NaHCO3
B. 逐滴滴加盐酸溶液,开始无气泡产生,则生成物一定含有Na2CO3
C. 加入BaCl2溶液,有白色沉淀,则可确定CO2和NaOH反应的离子方程式:CO2+2OH-==CO![]() +H2O
+H2O
D. 加入MgCl2溶液,有白色沉淀,则反应中NaOH溶液过量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
B. 强电解质一定是易溶于水的化合物,弱电解质一定是难溶于水的化合物
C. 水难电离,纯水是弱电解质
D. 溶于水能导电的化合物中一定含有阴阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的物质,它们之间有如图所示的转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。
![]()
(1)若A、B、C、W四种物质均为气体,其中A、W为单质,C的摩尔质量为46g/mol,则:
①B的化学式为_____________。
②实验室制取B时,______(填“能”或“不能”)用向上排空气法收集B。
③C与水反应的化学方程式为______________。
(2)若A为淡黄色固体单质,W为气体单质,B、C均为酸性氧化物,则:
①由B生成C时,每生成1molC,消耗W的物质的量为_________。
②C溶于水形成化合物D,在加热的条件下,D的浓溶液与A反应的化学方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TNT是一种烈性炸药,其结构简式如图所示,它是甲苯与浓硫酸、浓硝酸在一定条件下反应生成的.下列有关TNT的说法正确的是( ) 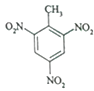
A.TNT分子式为C7H3O6N3
B.TNT的名称叫2,4,6﹣三硝基甲苯
C.每个TNT分子中可共平面的碳原子最多为6个
D.若硝酸的结构可表示为HO﹣NO2 , 每摩尔甲苯可取代3mol硝基制得TNT
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,反应 N2(g)+O2(g)2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是( )
A.缩小体积使压强增大
B.恒容,充入N2
C.恒容,充入He
D.恒压,充入He
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com