

| c(CO2)? c(H2) |
| c(CO)?c(H2O) |
| 3mol/L |
| 5min |

| 1.5mol |
| 6mol |
| c(CO2)? c(H2) |
| c(CO)?c(H2O) |
| 3��3 |
| 1��9 |

| x?x |
| (2-x)?(8-x) |


 ���������ʱ��ѵϵ�д�
���������ʱ��ѵϵ�д� �㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�㽭�¿γ���άĿ�������ʱ��ѵϵ�д� ��������ϵ�д�
��������ϵ�д� ���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 CO2��g��+H2��g��������5min��ﵽƽ��״̬������ʱ���H2��Ũ��Ϊ3mol?L-1����
CO2��g��+H2��g��������5min��ﵽƽ��״̬������ʱ���H2��Ũ��Ϊ3mol?L-1����| c(CO2)? c(H2) | c(CO)?c(H2O) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���ݻ�Ϊ0.5L���ܱ������У��� 2 mol CO��6mol H2O��ϼ��ȵ�800�棬������Ӧ��CO��g��+ H2O��g�� ![]() CO2��g��+ H2��g��������5min��ﵽƽ��״̬������ʱ���H2��Ũ��Ϊ3 mol��L-1����
CO2��g��+ H2��g��������5min��ﵽƽ��״̬������ʱ���H2��Ũ��Ϊ3 mol��L-1����
��1����CO��Ũ�ȱ仯��ʾ�ĸ÷�Ӧ�����ʡ�
��2����ƽ��ʱH2O��ת���ʡ�
��3����֪����һ���¶��£��÷�Ӧ��ƽ��ʱ�������ʵ�ƽ��Ũ��֮��������¹�ϵ��
![]()
�ҵ��¶Ȳ���ʱKΪ������K���淴Ӧ�������Ũ�ȵĸı���ı䡣��
����800���£��÷�Ӧ��K=�������� ��
����800���£���Ͷ��1 mol CO��4 mol H2O��ϼ��ȵ�ƽ��ʱ��H2Ũ���Ƕ��١�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��12�֣���һ���ݻ�Ϊ0.5L���ܱ������У��� 2 mol CO��6mol H2O��ϼ��ȵ�800�棬������Ӧ��CO��g��+ H2O��g�� ![]() CO2��g��+ H2��g��������5min��ﵽƽ��״̬������ʱ���H2��Ũ��Ϊ3 mol��L-1����
CO2��g��+ H2��g��������5min��ﵽƽ��״̬������ʱ���H2��Ũ��Ϊ3 mol��L-1����
��1����CO��Ũ�ȱ仯��ʾ�ĸ÷�Ӧ�����ʡ�
��2����ƽ��ʱH2O��ת���ʡ�
��3����֪����һ���¶��£��÷�Ӧ��ƽ��ʱ�������ʵ�ƽ��Ũ��֮��������¹�ϵ��
![]()
�ҵ��¶Ȳ���ʱKΪ������K���淴Ӧ�������Ũ�ȵĸı���ı䡣��
����800���£��÷�Ӧ��K= ��ww w.ks 5u.co m
����800���£���Ͷ��1 mol CO��4 mol H2O��ϼ��ȵ�ƽ��ʱ��H2Ũ���Ƕ��١�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2009-2010ѧ�꽭��ʡ�γ���ѧ��һ���£����л�ѧ�Ծ��������棩 ���ͣ������
 CO2��g��+H2��g��������5min��ﵽƽ��״̬������ʱ���H2��Ũ��Ϊ3mol?L-1����
CO2��g��+H2��g��������5min��ﵽƽ��״̬������ʱ���H2��Ũ��Ϊ3mol?L-1����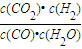
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com