
| A. | 可用向上排空气法收集氨气 | |
| B. | 氨气极易溶于水,因此加热浓氨水不会产生氨气 | |
| C. | 将两根分别蘸有浓氨水和浓硫酸的玻璃棒靠近时,有白烟产生 | |
| D. | 在实验室中,可用加热氢氧化钙和氯化铵的固体混合物的方法制取氨气 |
分析 A、氨气的密度小于空气;
B、浓氨水NH3•H2O很易分解;
C、浓硫酸是不挥发性酸;
D、Ca(OH)2和NH4Cl固体加热能发生复分解反应.
解答 解:A、氨气的密度小于空气,故应该用向下排空气法来收集,故A错误;
B、浓氨水NH3•H2O很易分解为氨气和水,故加热浓氨水时有NH3逸出,故B错误;
C、浓氨水易挥发出NH3,但浓硫酸是不挥发性酸,故两者不接触时,不会在两玻璃棒的中间生成白烟,故C错误;
D、Ca(OH)2和NH4Cl固体加热能发生复分解反应:Ca(OH)2+2NH4Cl$\frac{\underline{\;加热\;}}{\;}$CaCl2+2NH3↑+H2O,此反应是氨气的实验室制法,故D正确.
故选D.
点评 本题考查了氨气的实验室制法和性质,应注意的是氨气易溶于水的氨水,但氨水又易分解,故氨气和水的反应是可逆反应.


科目:高中化学 来源: 题型:选择题
| A. | 一定相同 | B. | 一定不同 | C. | 可能不同 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na和Na+的化学性质相似 | |
| B. | 钠在空气中燃烧生成氧化钠 | |
| C. | 钠可与硫酸铜溶液反应得到铜 | |
| D. | 实验室通常把钠保存在石蜡油或煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油、煤和天然气都是重要的化石燃料 | |
| B. | 淀粉、蔗糖和蛋白质均能发生水解反应 | |
| C. | 羊毛、塑料和橡胶均属于合成高分子材料 | |
| D. | 糖类、油脂和蛋白质都含有C、H、O三种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18gH2O所含的电子数目为9N0 | |
| B. | 0.1 mol/L Na2SO4溶液所含Na+数目为0.2N0 | |
| C. | 1 mol钠完全反应时所失去的电子数为N0 | |
| D. | 标准状况下22.4L O2所含的原子数目为N0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
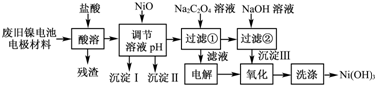
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,10L pH=12的Na2CO3溶液中含有的OH-离子数目为0.1NA | |
| B. | 50mL 18.4 mol/L浓硫酸与足量铜加热反应,生成SO2分子的数目为0.46NA | |
| C. | 1mol羟基(-OH)中含电子数为10NA | |
| D. | 4.6g 金属钠与足量乙醇反应放出2.24L氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验Na2CO3固体中是否混有NaHCO3,可向固体滴加稀盐酸,观察是否产生气体 | |
| B. | 焰色反应实验时,透过蓝色钴玻璃,可观察到Na+离子火焰呈黄色 | |
| C. | 欲证明某溶液中含有Fe3+,滴加KSCN溶液,可观察到溶液会变为血红色 | |
| D. | 向某无色溶液中加入BaCl2溶液有白色沉淀出现,再加入稀盐酸,沉淀不消失,则该溶液中一定含有SO${\;}_{4}^{2-}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com