
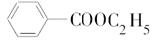 .
.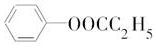 .
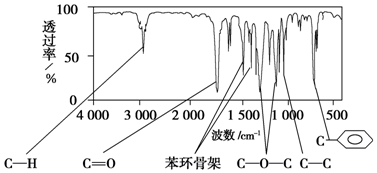
. 分析 (1)某有机物A的分子式为C9H10O2,A分子中只含一个苯环,且苯环上只有一个取代基,则苯环上的H的类型有3种,氢原子数目之比为1:2:2,其核磁共振氢谱有5个峰,面积之比为1:2:2:2:3,则另外的2个峰2:3来自侧链;A与NaOH溶液共热的两种生成物均可用于食品工业(常见防腐剂和饮品),结合A的红外光谱可知A分子中含有酯基,据此可判断A的结构;
(2)通过A的分子式和核磁共振氢谱可判断H的类型,从而确定含有甲基,而相对分子质量和红外光谱无法确定是否含有甲基;
(3)A的芳香类同分异构体有多种,其中符合下列条件:①分子结构中只含一个官能团,可能为羧基或酯基;②分子结构中含有一个甲基;③苯环上只有一个取代基,侧链为-OOCH2CH2CH3,或-CH2OOCCH3,或-COOCH2CH3,或-CH(CH3)OOCH,或-CH(CH3)COOH;水解产物能使FeCl3溶液变紫色,说明分子中含有酚羟基,据此判断满足体积的有机物的结构简式.
解答 解:(1)机物A的分子式为C9H10O2,A分子中只含一个苯环,且苯环上只有一个取代基,则苯环上的H的类型有3种,氢原子数目之比为1:2:2,其核磁共振氢谱有5个峰,面积之比为1:2:2:2:3,则另外的2个峰2:3来自侧链;A与NaOH溶液共热的两种生成物均可用于食品工业(常见防腐剂和饮品),结合A的红外光谱可知A分子中含有酯基,则A为苯甲酸乙酯,其结构简式为: ,
,
故答案为: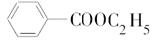 ;
;
(2)通过A的分子式C9H10O2及核磁共振氢谱有5个峰,面积之比为1:2:2:2:3可确定A分子中含有1个甲基,而A的相对分子质量、红外光谱都无法确定是否含有甲基,故bc正确,
故答案为:bc;
(3)A的芳香类同分异构体有多种,其中符合下列条件:①分子结构中只含一个官能团,可能为羧基或酯基;②分子结构中含有一个甲基;③苯环上只有一个取代基,侧链为-OOCH2CH2CH3,或-CH2OOCCH3,或-COOCH2CH3,或-CH(CH3)OOCH,或-CH(CH3)COOH,共有5种;
其中水解产物能使FeCl3溶液变紫色,说明有机物分子水解产物中含有酚羟基,其结构简式为: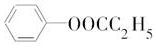 ,
,
故答案为:5;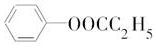 .
.
点评 本题考查有机物结构与性质,题目难度中等,正确推断A的结构为解答关键,注意熟练掌握常见有机物组成、结构与性质,试题有利于提高学生的分析、理解能力及逻辑推理能力.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 晶体硅是良好的半导体材料 | |
| B. | 铁、铝合金的熔点高于铁的熔点,硬度小 | |
| C. | 氨常用作制冷剂利用了氨的化学性质 | |
| D. | 漂白粉、明矾都可用于污水的净化,其原理是相同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2 | B. | CH≡C-CH3 | C. | CH2=CH-CH=CH2 | D. | CH3-CH=CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 0.1mol/LNaClO溶液/mL | 0.1mol/LNaCl溶液/mL | 0.2mol/LNaOH溶液/mL | H2O/mL | 品红溶液 | 现象 |
| ① | 4.0 | 0 | 0 | x | 3滴 | 较快褪色 |
| ② | 0 | 4.0 | 4.0 | 0 | 3滴 | 不褪色 |
| ③ | 4.0 | 0 | 4.0 | 0 | 3滴 | 缓慢褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
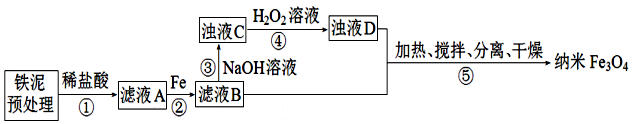
| 沉淀物 | Fe(OH)3 | Fe(OH)2 |
| 完全沉淀物PH | 3.0 | 8.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 催化剂V2O5不改变该反应的逆反应速率 | |
| B. | 不论以何种方式使反应体系的压强增大,化学反应速率一定增大 | |
| C. | 该反应是放热反应,降低温度将缩短反应到达平衡的时间 | |
| D. | 当该反应到达平衡时,SO2、O2、SO3都存在于反应体系中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2O?H3O++OH- | B. | H2S?H++HS- | C. | NaHS=Na++HS- | D. | HCO3-=H++CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com