
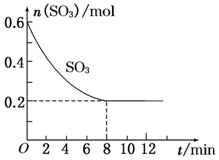
 在一个2.0L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的变化如图所示:
在一个2.0L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的变化如图所示:分析 (1)化学平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比;
(2)先计算三氧化硫的平均反应速率,再根据同一可逆反应中同一时间段内各物质的计量数之比等于其反应速率之比计算氧气反应速率;
(3)8min时反应达平衡状态,此时SO3的转化率=$\frac{消耗量}{起始量}$×100%;
(4)升高温度,反应速率增大,平衡向吸热反应方向移动,该反应的正反应是吸热反应,所以升高温度平衡向正反应方向移动,平衡常数增大;
(5)可逆反应达到平衡状态时正逆反应速率相等,各物质的物质的量不变、物质的量浓度不变、百分含量不变以及由此引起的其它物理量不变;
(6)在第12min时,容器压缩到1L,增大压强,平衡向气体体积减小的方向移动.
解答 解:(1)由2SO3(g)?2SO2(g)+O2(g)可知化学平衡常数K=$\frac{{c}^{2}(S{O}_{2})c({O}_{2})}{{c}^{2}(S{O}_{3})}$,故答案为:$\frac{{c}^{2}(S{O}_{2})c({O}_{2})}{{c}^{2}(S{O}_{3})}$;
(2)三氧化硫平均反应速率=$\frac{\frac{(0.6-0.2)mol}{2L}}{8min}$=0.025mol/(L•min),同一可逆反应中同一时间段内各物质的计量数之比等于其反应速率之比,所以二氧化硫反应速率为0.025 mol/(L•min),故答案为:0.025 mol/(L•min);
(3)8min时反应达平衡状态,此时SO3的转化率=$\frac{消耗量}{起始量}$×100%=$\frac{(0.6-0.2)mol}{0.6mol}$×100%=66.7%,
故答案为:66.7%;
(4)升高温度正逆反应速率都增大,该反应的正反应是吸热反应,升高温度平衡向正反应方向移动,则K增大,故答案为:增大;增大;
(4)A.n(SO3):n(SO2):n(O2)=2:2:1,反应不一定达到平衡状态,所以不能据此判断平衡状态,故A错误;
B.该反应是一个反应前后气体体积改变的可逆反应,当容器内压强保持不变时该反应达到平衡状态,故B正确;
C.v(SO2)逆=2v(O2)正 ,正逆反应速率相等,则该反应达到平衡状态,故C正确;
D.容器内气体质量、气体体积始终不变,则密度始终保持不变,所以不能据此判断平衡状态,故D错误;
故选B、C,
故答案为:BC;
(6)在第12min时,容器压缩到1L,体积减小的瞬间,三氧化硫物质的量不变、物质的量浓度增大,增大压强,平衡向气体体积减小的方向移动,则向逆反应方向移动,
故答案为:逆反应;压强增大平衡向气体体积减小的方向移动;
点评 本题考查较综合,涉及平衡计算、平衡状态的判断、平衡移动等知识点,侧重考查计算、基本理论,知道只有反应前后改变的物理量才能作为判断平衡状态的依据,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
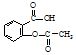 )具有解热镇痛作用(选填“解热镇痛”或“抗菌消炎”),必须密闭干燥存储以防止发生水解,在酸性条件下阿司匹林水解生成乙酸和
)具有解热镇痛作用(选填“解热镇痛”或“抗菌消炎”),必须密闭干燥存储以防止发生水解,在酸性条件下阿司匹林水解生成乙酸和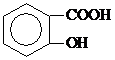 (写出结构简式).
(写出结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:实验题
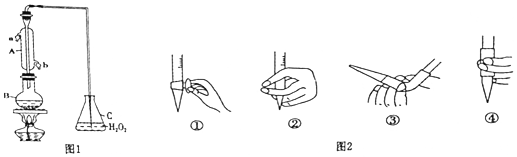
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K1=2K2 | B. | K1=K22 | C. | K1=K2 | D. | K1=$\sqrt{{K}_{2}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(2)(3)(5) | B. | (1)(3)(5) | C. | (2)(3)(6) | D. | (1)(3)(4)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 Na2SO3•7H2O是食品工业中常用的漂白剂、抗氧化剂和防腐剂.该小组同学用Na2SO3与浓硫酸制备SO2,并把SO2通入NaNO3溶液中,他们为了检验产生的气体是NO还是
Na2SO3•7H2O是食品工业中常用的漂白剂、抗氧化剂和防腐剂.该小组同学用Na2SO3与浓硫酸制备SO2,并把SO2通入NaNO3溶液中,他们为了检验产生的气体是NO还是查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的三氯代物一共有 5 种 | |
| B. | 乙烯和乙酸均能发生加成反应 | |
| C. | 乙烷通入氯水中能发生取代反应 | |
| D. | 淀粉和纤维素都属于天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com