
【题目】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X元素与Y元素最高正价与最低负价之和均为0;元素Q的离子与![]() 所含的电子数和质子数均相同;Z、R分别是地壳中含量最高的非金属元素和金属元素。
所含的电子数和质子数均相同;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子的半径由大到小的顺序是(写元素符号)____________。
(2)X与Z形成的一种化合物,既含极性键又含非极性键,则化合物的化学式是_________,该化合物具有很强的氧化性,写出其与SO2反应的化学方程式:____________________;此化合物在某些反应中也可表现还原性,写出其与酸性高锰酸钾反应的离子方程式:_______________。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A![]() B(在水溶液中进行)其中C是溶于水显酸性的气体;D是黄色固体。写出D的电子式:_____________;如果A、B均由三种元素组成,B为两性不溶物,则该A的化学式为______________;由A与少量C反应生成为B的离子方程式为_________________。
B(在水溶液中进行)其中C是溶于水显酸性的气体;D是黄色固体。写出D的电子式:_____________;如果A、B均由三种元素组成,B为两性不溶物,则该A的化学式为______________;由A与少量C反应生成为B的离子方程式为_________________。
【答案】 Na>Al>C>O>H H2O2 H2O2+SO2=H2SO4 2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O ![]() NaAlO2 2AlO2-+CO2+H2O=2Al(OH)3+CO32-
NaAlO2 2AlO2-+CO2+H2O=2Al(OH)3+CO32-
【解析】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。Z、R分别是地壳中含量最高的非金属元素和金属元素,则Z为O元素、R为Al;X、Y元素最高正价与最低负价之和均为0,氢元素、ⅣA族元素符合,由原子序数可知,X为H元素,Y为C元素;元素Q的离子与![]() 所含的电子数和质子数均相同,Q原子序数大于氧,可知Q为Na,则
所含的电子数和质子数均相同,Q原子序数大于氧,可知Q为Na,则
(1)所有元素中H原子半径最小,同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径:Na>Al>C>O>H;(2)X与Z形成的一种化合物,既含极性键又含非极性键,则化合物是双氧水,化学式是H2O2,双氧水具有很强的氧化性,与SO2反应的化学方程式为H2O2+SO2=H2SO4;双氧水也可表现还原性,与酸性高锰酸钾反应的离子方程式为2MnO4+5H2O2+6H+=2Mn2++5O2+8H2O;(3)上述五种元素中的若干种组成的化合物A、B、C、D,其中C是溶于水显酸性的气体,D是淡黄色固体,则C为CO2、D为Na2O2,Na2O2是离子化合物,电子式为![]() ;如果A、B均由三种元素组成,B为两性不溶物,结合转化关系可知,A为NaAlO2、B为Al(OH)3,偏铝酸根与二氧化碳、水反应生成氢氧化铝与碳酸根,A与少量C反应生成为B的离子方程式为2AlO2+CO2+H2O=2Al(OH)3+CO32。
;如果A、B均由三种元素组成,B为两性不溶物,结合转化关系可知,A为NaAlO2、B为Al(OH)3,偏铝酸根与二氧化碳、水反应生成氢氧化铝与碳酸根,A与少量C反应生成为B的离子方程式为2AlO2+CO2+H2O=2Al(OH)3+CO32。


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是
A.容量瓶中原有少量的蒸馏水
B.移液时,不慎将液体流到瓶外
C.容量瓶盛过KOH溶液,使用前未洗涤
D.定容时仰视刻度线和液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25 ℃条件下向10.00 mL 0.1 mol·L-1CH3COOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如下图所示(忽略温度变化)。下列说法中不正确的是( )
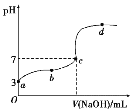
A.a点表示的溶液中c(CH3COO-)约为10-3 mol·L-1
B.用25 .00mL的酸式滴定管量取CH3COOH溶液
C.c点NaOH溶液的体积小于10 mL
D.在a、c间任一点,溶液中一定都有c(Na+)>cCH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素。下列判断正确的是( )

A. 甲一定是金属元素
B. 气态氢化物的稳定性:庚>己>戊
C. 乙、丙、丁的最高价氧化物水化物可以以相互反应
D. 庚的最高价氧化物水化物酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体和溶液的说法中,不正确的是( )
A. 胶体和溶液都是均一、稳定的分散系,静置不易产生沉淀
B. 蔗糖、淀粉、蛋白质的水溶液均能产生丁达尔效应
C. 光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应
D. 向Fe(OH)3胶体中逐滴加入稀硫酸先产生沉淀而后沉淀逐渐溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同位素常用做环境分析指示物,下列对同位素的说法正确的是( )
A.34S原子核内的中子数为16
B.13C和15N原子核内的质子数相差2
C.16O与18O的核电荷数相等
D.2H+质量与1H+的质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的离了,能在溶液中大量共存的是( )
A. SO42-、Na+、Cl-、Ba2+ B. H+、Fe2+、NO3-、OH-
C. H+、K+、CO32-、HCO3- D. Na+、Cu2+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高聚物--CH2—CH2—CH2-是用下列何种物质聚合而成的:
A.CH3-CH3 B.CH3-CH2-CH3 C.CH2=CH-CH3 D.CH2=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届天水市一中期末】钠、钾的碘化物在生产和科学实验中有十分重要的应用。工业利用碘、NaOH和铁屑为原料可生产碘化钠,其生产流程如图所示:
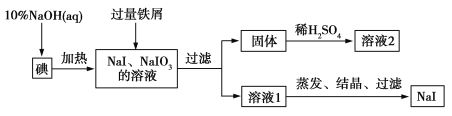
(1)NaOH溶液和碘反应时需要严格控制温度,如果温度过低,会生成碘的低价副产品NaIO。若NaOH溶液和碘反应时所得溶液中IO![]() 与IO-的物质的量之比为1∶1,则该反应的离子方程式为______ 。
与IO-的物质的量之比为1∶1,则该反应的离子方程式为______ 。
(2)生产流程中加入过量铁屑的目的是__________________,过滤所得固体中除剩余铁屑外,还有红褐色固体,则加入铁屑时发生反应的化学方程式是________ __________。
(3)溶液2中除含有H+外,一定含有的阳离子是______ ____________;试设计实验证实该金属阳离子的存在:__________________________________。
(4)溶液2经一系列转化可以得到草酸亚铁晶体(FeC2O4·2H2O),称取3.60 g草酸亚铁晶体(相对分子质量是180)用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示:
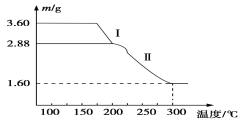
①分析图中数据,根据信息写出过程I发生的化学方程式:____________ ______。
②300℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式:________ ________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com