
科目:高中化学 来源: 题型:
反应A(g)+B(g)―→C(g) ΔH,分两步进行:①A(g)+B(g)―→X(g) ΔH1 ②X(g)―→C(g) ΔH2,反应过程中能量变化如图所示,E1表示A+B―→X的活化能,下列说法正确的是( )
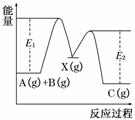
A.ΔH1=ΔH-ΔH2>0
B.X是反应A(g)+B(g)―→C(g)的催化剂
C.E2是反应②的活化能
D.ΔH=E1-E2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气后都首先发生置换反应
B.XCl3的溶液能与铜片发生反应,则铜的金属性一定比X强
C.非金属X能将Fe氧化到+3价,但非金属Y不能,则Y的氧化性一定比X强
D.Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化
查看答案和解析>>
科目:高中化学 来源: 题型:
已知分解1mol H2O2放出热量98kJ。在含有少量I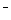 的溶液中,H2O2分解的机理为:
的溶液中,H2O2分解的机理为:
 H2O2+ I
H2O2+ I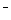
 H2O+IO
H2O+IO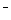
H2O2+ IO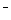
 H2O+O2+ I
H2O+O2+ I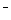
下列有关该反应的说法正确的是( )
A.反应速率与I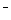 浓度有关 B.IO
浓度有关 B.IO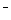 也是该反应的催化剂
也是该反应的催化剂
C.反应活化能等于98kJ·mol-1 D.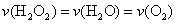
查看答案和解析>>
科目:高中化学 来源: 题型:
3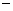 对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
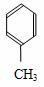 +CO
+CO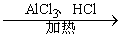 A
A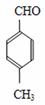
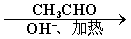 B
B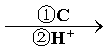
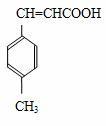
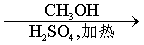 E
E
已知:HCHO+CH3CHO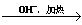 CH2=CHCHO+H2O。
CH2=CHCHO+H2O。
(1)遇FeCl3溶液显紫色的A的同分异构体有_______种。B中含氧官能团的名称为_____________。
(2)1molB最多能跟______mol H2发生加成反应。
H2发生加成反应。
(3)试剂C可选用下列中的_____________。
a、溴水 b、银氨溶液 c、酸性KMnO4溶液 d、新制Cu(OH)2悬浊液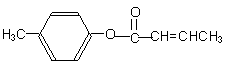
(4) 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为__________________________________。
(5)E在一定条件下可以生成高聚物F,F的结构简式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
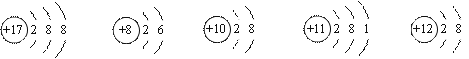 |
A B C D E
(1)属于阴离子结构示意图的是 ▲ (填字母编号)。
(2)性质最稳定的原子是 ▲ (填字母编号)。
(3)元素D的单质在B2中燃烧,该产物的化学式 ▲ 。
(4)在核电荷数1-18的元素内,列举一个与C原子的电子层结构相同的离子,写
出离子的符号 ▲ 。
(5)写出化合物DAB在水溶液中的电离方程式 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应原理在科研和生产中有广泛应用。
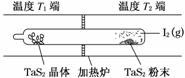
(1)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应:
TaS2(s)+2I2(g)TaI4(g)+S2(g) ΔH>0 (Ⅰ)
反应(Ⅰ)的平衡常数表达式K=________,若K=1,向某恒容容器中加入1 mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为________。
(2)如图所示,反应(Ⅰ)在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净TaS2晶体,则温度T1________T2(填“>”、“<”或“=”)。上述反应体系中循环使用的物质是________。
(3)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为________,滴定反应的离子方程式为________________________________________________________________________。
(4)25℃时,H2SO3HSO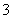 +H+的电离常数Ka=1×10-2 mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kb=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中
+H+的电离常数Ka=1×10-2 mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kb=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中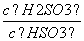 将________(填“增大”、“减小”或“不变”)。
将________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com