
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4∶3,Z原子比X原子的核外电子数多4。下列说法正确的是( )
A.W、Y、Z的电负性大小顺序一定是Z>Y>W
B.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z
C.Y、Z形成的分子空间构型可能是正四面体
D.WY2分子中含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语使用正确的是( )
A.硫原子的原子结构示意图: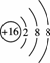
B.NH4Cl的电子式:[H

 H]+Cl-
H]+Cl-
C.原子核内有10个中子的氧原子: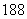 O
O
D.对氯甲苯的结构简式:ClCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是短周期中部分元素的原子半径及主要化合价。
| 元素代号 | U | V | W | X | Y | Z |
| 原子半径/nm | 0.037 | 0.157 | 0.066 | 0.070 | 0.077 | 0.143 |
| 主要化合价 | +1 | +1 | -2 | -3 +5 | +2 +4 | +3 |
请回答:
(1)X在元素周期表中的位置是 第二周期ⅤA族 。
(2)V、W、Z三种元素的离子具有相同的电子层结构,三者的离子半径由大到小顺序是O2->Na+>Al3+ (用离子符号表示)。用离子方程式表示出Z离子可作净水剂的原因:________________________________________________________________________
________________________________________________________________________。
(3)某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的电子式: Na+[
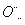
 H]- 。2·1·c·n·j·y
H]- 。2·1·c·n·j·y
(4)1 g YU4气体完全燃烧生成液态水时,放出a kJ的热量,则该反应的热化学方程式为________________________________________________________________________
________________________________________________________________________。
(5)现有Z与V2W2的固体混合物样品,加入稀盐酸至混合物完全溶解,所得的混合液中c(Z3+)∶c(H+)∶c(Cl-)=1∶2∶8,则原固体混合物中,Z元素与W元素的质量比为 9∶16 (最简整数比)。【来源:21·世纪·教育·网】
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关晶体的说法中正确的是
A.氯化钾溶于水时离子键未被破坏 B.原子晶体中共价键越强,熔点越高
C.冰融化时分子中共价键发生断裂 D.范德华力越大,分子越稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是
A.对羟基苯甲酸的沸点比邻羟基苯甲酸高,冰中既存在范德华力,又存在氢键
B.简单立方是非密置层三维堆积形成的,面心立方是由密置层三维堆积形成的
C.所有共价键都有方向性,形成氢键的三个相关原子可以不在直线上
D.金属晶体的导电、导热性都与自由电子有关,离子晶体在一定条件下可以导电
查看答案和解析>>
科目:高中化学 来源: 题型:
LiPF6是锂离子电池中广泛应用的电解质。某工厂用LiF、PCl5为原料,低温反应制备LiPF6,其流程如下:
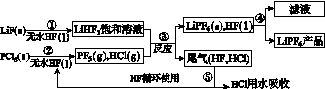
已知:HCl的沸点是-85.0 ℃,HF的沸点是19.5 ℃。
(1)第①步反应中无水HF的作用是________________、________________。反应设备不能用玻璃材质的原因是______________________________________________(用化学方程式表示)。无水HF有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的________溶液冲洗。
(2)该流程需在无水条件下进行,第③步反应中PF5极易水解,其产物为两种酸,写出PF5水解的化学方程式:____________________________________。
(3)第④步分离采用的方法是________;第⑤步分离尾气中HF、HCl采用的方法是________。
(4)LiPF6产品中通常混有少量LiF。取样品w g,测得Li的物质的量为n mol,则该样品中LiPF6的物质的量为________mol(用含w、n的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com