
���� �ɹ������̼�֪�������������ᷴӦ�ù���AΪ��ҺB�������AΪSiO2����ҺB�����Ȼ������Ȼ������Ȼ�þ�ȣ���Һ�м��������NaOH������֪����CΪ����������������þ����ҺD����ƫ�����ơ��Ȼ��ơ�NaOH����������ҺD��ͨ�����������̼��������������������̼�����ƣ�����FΪAl��OH��3����ҺE�к���NaCl��NaHCO3��
���ݹ��������ҿ�֪���������е�Al2O3��SiO2�ܺ��������Ʒ�Ӧ����֪����XΪFe2O3��MgO�ȣ���ҺYΪ�����ơ�ƫ�����ƣ���Һ��ͨ�����������̼������ZΪAl��OH��3�����ᣬ��ҺK�к���NaHCO3���Դ������
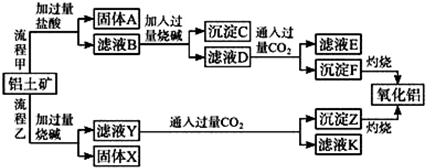
��� �⣺�ɹ������̼�֪�������������ᷴӦ�ù���AΪ��ҺB�������AΪSiO2����ҺB�����Ȼ������Ȼ������Ȼ�þ�ȣ���Һ�м��������NaOH������֪����CΪ����������������þ����ҺD����ƫ�����ơ��Ȼ���NaOH����������ҺD��ͨ�����������̼��������������������̼�����ƣ�����FΪAl��OH��3����ҺE�к���NaCl��NaHCO3��
���ݹ��������ҿ�֪���������е�Al2O3��SiO2�ܺ��������Ʒ�Ӧ����֪����XΪFe2O3��MgO�ȣ���ҺYΪ�����ơ�ƫ�����ƣ���Һ��ͨ�����������̼������ZΪAl��OH��3�����ᣬ��ҺK�к���NaHCO3��
��1������ҺY��ͨ������CO2ʱ���ɵij���ZΪAl��OH��3�����ᣬ������Ӧ�����ӷ���ʽΪ��SiO32-+2CO2+2H2O=H2SiO3��+2HCO3-��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
�ʴ�Ϊ��SiO32-+2CO2+2H2O=H2SiO3��+2HCO3-��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
��2����֤��ҺB��Fe3+����ȡ������Һ���������軯����Һ������Һ�Ƿ��Ѫ��ɫ��
�ʴ�Ϊ�����軯����Һ��
��3����ҵ�ϳ��õ���������ķ���ұ������
�ʴ�Ϊ��ұ������
��4����������ķ�����֪�������ҵõ�ZΪAl��OH��3�����ᣬ���ȷֽ�õ����������к��ж����������ʣ�
�ʴ�Ϊ���������к��ж����������ʣ�
��5���������뽹̿�Ļ�����ڵ����и��¼��ȷ�Ӧ���Ƶ����ͷǽ�������AlN��һ����ѧ��������X������Ԫ���غ��֪X��Ӧ������Ԫ�غ�̼Ԫ�أ���֪ÿת��6.02��1023�����Ӽ�1mol���ӣ���0.5mol������X���ɣ��ɵ���ת���غ㣬�ɵ���X��C�Ļ��ϼ�Ϊ$\frac{1mol}{0.5mol}$=2������X��CO�����Ը÷�Ӧ�Ļ�ѧ����ʽΪAl2O3+N2+3C$\frac{\underline{\;����\;}}{\;}$2AlN+3CO��
�ʴ�Ϊ��Al2O3+N2+3C$\frac{\underline{\;����\;}}{\;}$2AlN+3CO��
���� ��������������ȡ��������Ϊ���忼���������ʵ�鷽������ƣ�Ϊ��Ƶ���㣬�漰�����ƶϡ�Ԫ�ػ��������ʼ��ת�������ӵķ��������ӷ���ʽ�ȣ����ط�����ʵ�������Ŀ��飬��Ŀ�Ѷ��еȣ�


 Сѧ���AB��ϵ�д�
Сѧ���AB��ϵ�д� ABC����ȫ�ž�ϵ�д�
ABC����ȫ�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�ѧ����ʽ�У���ѧʽǰ��Ļ�ѧ�������ȿɱ�ʾ�������ֿɱ�ʾ���ʵ��� | |
| B�� | ͬ��ͬѹ�£�H2��g��+Cl2��g���T2HCl��g���ڹ��պ͵�ȼ�����µġ�H��ͬ | |
| C�� | ��д�Ȼ�ѧ����ʽʱ������Ҫд����Ӧ�ȣ���Ҫע�������ʵľۼ�״̬ | |
| D�� | ���ǻ��Ϸ�Ӧ���Ƿ��ȷ�Ӧ���ֽⷴӦ�������ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����2 min��AŨ�ȼ�����0.8 mol/L | |
| B�� | �ֱ���B��C��D��ʾ�ķ�Ӧ���ʵı�ֵΪ3��2��1 | |
| C�� | ��2 minĩ�ķ�Ӧ���ʣ���B��ʾ�ǣ�0.3 mol/��L•min�� | |
| D�� | ����2 min����D��ʾ�Ļ�ѧ��Ӧ����Ϊ��0.2mol/��L•min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �˷�Ӧ��ˮ�Ȳ����������ֲ��ǻ�ԭ�� | |
| B�� | �Թ�����Һ�����ʵ����ʵ���Ũ��Ϊ$\frac{1}{22.4}$mol/L | |
| C�� | ��Һ���ռ�Թ��ݻ�������֮�� | |
| D�� | �����Թ��е����廻Ϊ�Ȼ�����߰�������ˮ�����Թ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
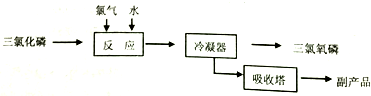
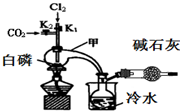 ���Ȼ��ף�$\stackrel{+3}{P}$Cl3�����������ף�POCl3����������ˮ��ǿ��ˮ������ʣ�PCl3�Ǻϳ�ҩ�����Ҫ����ԭ�ϣ�POCl3������ȡȾ���м��壬�л��ϳɵ��Ȼ�������������ȼ�������������뵼����Ӽ������άԭ�ϣ�
���Ȼ��ף�$\stackrel{+3}{P}$Cl3�����������ף�POCl3����������ˮ��ǿ��ˮ������ʣ�PCl3�Ǻϳ�ҩ�����Ҫ����ԭ�ϣ�POCl3������ȡȾ���м��壬�л��ϳɵ��Ȼ�������������ȼ�������������뵼����Ӽ������άԭ�ϣ�| ���� | �۵�/�� | �е�/�� | �ܶ�/g•cm-3 |
| ���� | 44.1 | 280.5 | 1.82 |
| PCl3 | -112 | 75.5 | 1.574 |
| POCl3 | 2 | 105.3 | 1.675 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaOH��Һ�����ĥ�ڲ��������Լ�ƿ | |
| B�� | Һ��Ӧ��������ɫĥ�ڲ��������Լ�ƿ�У���������ˮ����ˮ�� | |
| C�� | Ϊ��ֹ��������FeSO4��Һ����ڼ����������۵��Լ�ƿ�� | |
| D�� | ����Ӧװ����ɫƿ���ܷ�ܹⱣ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ij��ɫ��Һ�м�BaCl2��Һ����������ϡHNO3�İ�ɫ������˵��ԭ��Һ��һ����SO42- | |
| B�� | ��ij��ɫ��Һ�м������ᣬ����ɫ��ζ�������������˵��ԭ��Һ��һ����CO32- | |
| C�� | ��ij��Һ�еμ�KSCN��Һ����Һ����죬�ٵμ���ˮ����죬˵��ԭ��Һһ����Fe2+ | |
| D�� | ��ij��ɫ��Һ�м�ŨNaOH��Һ�����ȣ�������ʹʪ�����ɫʯ����ֽ�������壬��˵��ԭ��Һ��һ����NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��0.2mol H2SO4��Ũ����������Cu�ڼ��������·�Ӧ������SO2�ķ�����Ϊ0.1NA | |
| B�� | ��״����11.2L O3��CO2��������к�ԭ����Ϊ1.5NA | |
| C�� | 100mL 2mol•L-1��NaHSO3��Һ�У�HSO3-��SO32-��Ŀ֮��Ϊ0.2NA | |
| D�� | KClO3+6HCl��Ũ���TKCl+3Cl2��+3H2O�У�����1.5mol Cl2ת�Ƶ�����Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ա�̼���� | B�� | ����ʹ��ɫʯ����Һ��� | ||
| C�� | ������ˮ | D�� | �ܱ�����Ϊ��ȩ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com