
下列反应可用于检验司机是否酒后驾车,
2K2Cr2O7+3CH3CH2OH+8H2SO4![]() 2Cr2(SO4)3+3CH3COOH+2K2SO4+□□
2Cr2(SO4)3+3CH3COOH+2K2SO4+□□
(橙红色) (红色)
(1)□□内所缺其化学计量数及物质为________(写化学式).
(2)该反应中,氧化剂是________,氧化产物是________,铬元素的化合价从________价变到了________价.
科目:高中化学 来源: 题型:阅读理解
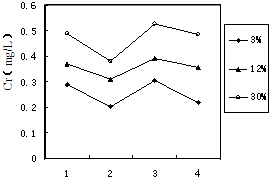 铬(Cr)属于重金属元素,含铬废水和废渣排放必须经过处理达到有关的安全标准.
铬(Cr)属于重金属元素,含铬废水和废渣排放必须经过处理达到有关的安全标准.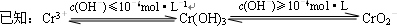 ①FeSO4还原Cr2O72-的离子方程式为
①FeSO4还原Cr2O72-的离子方程式为查看答案和解析>>
科目:高中化学 来源:高中化学新课标鲁科版 必修Ⅱ 鲁科版 题型:022
下列反应可用于检验司机是否酒后驾车.
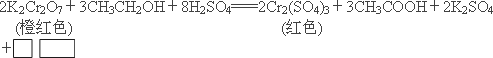
(1)![]() 内所缺其计量数及物质为________(写分子式).
内所缺其计量数及物质为________(写分子式).
(2)该反应中,氧化剂是________,氧化产物是________,铬元素的化合价从
价变到了________价.
查看答案和解析>>
科目:高中化学 来源: 题型:
![]()
(1)![]() 内所缺其化学计量数及物质为___________________(写化学式)。
内所缺其化学计量数及物质为___________________(写化学式)。
(2)该反应中,氧化剂是_________________,氧化产物是_______________,铬元素的化合价从_______________价变到了_______________价。
查看答案和解析>>
科目:高中化学 来源: 题型:
2K2Cr2O7(橙红色)+3C2H5OH+8H2SO4==2Cr2(SO4)3(绿色)+3CH3COOH+2K2SO4+11![]()
(1)方程式中空格内的物质是(写化学式)________________________。
(2)若司机酒后开车,则显示_________色。
(3)反应中铬元素的化合价从_________价变为_________价。
(4)如果反应中生成1 mol Cr3+,转移的电子总数约是_________个。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com