
下列试剂中,不能使Fe2+转化为Fe3+的是 ( )
①氯气 ②NaCl溶液 ③KMnO4溶液 ④稀硝酸 ⑤盐酸 ⑥NaNO3溶液
A.①②③ B.①③④ C.②④⑤ D.②⑤⑥
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A、沸点大小关系为: 乙酸>水>乙醇>溴乙烷>甲醛
B、在水中溶解度大小关系为:乙酸异戊酯<苯酚<乙醇
C、用水可以区别苯、乙醛、四氯化碳、醋酸、硝基苯五种液体
D、甲醛、乙酸任意比混合,等质量的混合物完全燃烧耗氧量和生成CO2量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
氨溴索是呼吸道润滑祛痰药,先广泛用于慢性支气管炎、支气管扩张、支气管哮喘、肺结核、术后咳痰困难等,其合成路线如下:
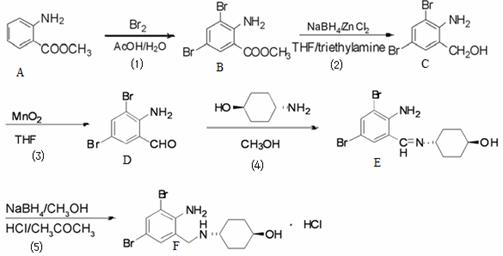
请回答一下问题:
(1)化合物A含有的官能团为 、 (填写官能团名称);
(2)属于取代反应的是 (填编号);
(3)写出步骤(3)的化学反应方程式 ;
(4)写出符合下列要求的化合物A的同分异构体 (任写一种);
①属于芳香族化合物 ②取代基团在对位 ③不能发生水解 ④有3种环境H元素
(5)写出以甲苯为原料(其他试剂任选)合成邻氨基苯甲酸甲酯的合成路线流程图
①已知:苯环取代基定位基团中甲基是邻对位定位基团;—NO2在Fe/HCl条件下还原成—NH2
②合成路线流程图示例如下:
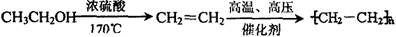
查看答案和解析>>
科目:高中化学 来源: 题型:
由FeO、Fe2O3和Fe3O4组成的混合物,测得其中铁元素与氧元素的质量比为21∶8,则这种混合物中FeO、Fe2O3和Fe3O4的物质的量之比是 ( )
A.1∶2∶1 B.2∶1∶1
C.1∶3∶1 D.1∶1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各离子组能大量共存的是 ( )
A.Fe3+、NH 、H+、SO
、H+、SO
B.Fe3+、Br-、Na+、I-
C.Fe2+、[Al(OH)4]-、Na+、NO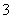
D.Fe3+、HCO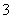 、NH
、NH 、NO
、NO
查看答案和解析>>
科目:高中化学 来源: 题型:
在含有Fe3+、Fe2+、Al3+、NH 的稀溶液中加入足量Na2O2固体,充分反应后,再加入过量稀盐酸,完全反应,则离子数目没有变化的是 ( )
的稀溶液中加入足量Na2O2固体,充分反应后,再加入过量稀盐酸,完全反应,则离子数目没有变化的是 ( )
A.Fe3+、Al3+ B.Al3+
C.Fe2+、NH D.Fe3+
D.Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式或离子方程式中,正确的是:
A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H= -890.3kJ·mol-1
B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:

 △H=-38.6kJ·mol-1
△H=-38.6kJ·mol-1
C.氯化镁溶液与氨水反应: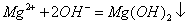
D.氧化铝溶于NaOH溶液: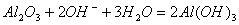

查看答案和解析>>
科目:高中化学 来源: 题型:
由A[b18] 、D、E、G四种微粒组成的复盐W的化学式为xAaDd·yE2D·zG。4.704gW溶于水得一澄清的弱酸性溶液,其中溶质总量为3.408g。同质量的W与5.13g氢氧化钡充分混匀后加热,生成的气体以足量铝盐溶液充分吸收得Al(OH)3 0.624g,加热后的残渣用水充分溶解后过滤,滤液以酚酞为指示剂用0.400mol/L H2SO4滴定至终点,用去H2SO4 15.0mL,滴定完毕后,溶液中检测不出任何金属离子和酸根离子;滤渣用硝酸洗涤时部分溶解,得一遇石炭酸显紫色的黄色溶液,依据推理和计算判断:
(1)依次写出D、E、G三种微粒符号___▲ _____、___▲ ____、____▲ _____;
(2)a、d的比值为____▲ _____;
(3)复盐的化学式为___▲ _____。(写出计算步骤)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com