
某研究性学习小组计划研究当地酸雨的形成过程,于是取来雨水作水样进行测定,随时间的推移,多次测定该样品的pH,得到如下数据:
| 时间(h) | 开始 | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(1)雨水样品放置时pH变化的主要原因为______________________________________
(用化学方程式表示 )。由此可以得出酸雨的形成过程可能是_______________________。
)。由此可以得出酸雨的形成过程可能是_______________________。
如果将刚取样的上述雨水和自来水相混合,pH将______(填“增大”、“减小”或“不变”),原因是________________________ __________________________________,
__________________________________,
二氧化硫表现________性。
(2)下面是酸雨给人类造成的危害,其中不正确的是___________________________。
A.腐蚀建筑物、雕塑等 B.污染水源
C.改良碱性土壤 D.损害庄稼
(3)你认为减少酸雨产生的途径可采取的措施是_____________________________。
①少用煤作燃料 ②把工厂的烟囱造高 ③燃料脱硫
④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤
C.①③⑤ D.①③④⑤
答案 (1)2H2SO3+O2===2H2SO4 雨水溶解二氧化硫生成亚硫酸,亚硫酸又被空气中的氧气氧化为硫酸,降落下来形成酸雨 减小 自来水中的氯气(或次氯酸)把亚硫酸氧化成硫酸 还原 (2)C (3)C
解析 酸雨的pH发生变化,其原因是亚硫酸被空气中的氧气氧化为硫酸,酸性增强,当亚硫酸全部氧化为硫酸后,pH不再变化。自来水常用氯气消毒,其中的氯气、次氯酸等能把亚硫酸氧化为硫酸,使pH减小。酸雨的危害极大,会危害农作物、森林、草原、鱼类、建筑物、工业设备、电信电缆等。要减少酸雨的产生,首先要了解大气中二氧化硫的来源。大气中二氧化硫的来源主要是化石燃料的燃烧、含硫矿石的冶炼和硫酸、磷肥、造纸等生产过程中产生的尾气。因此少用煤作燃料以及对燃料进行脱硫处理,是减少酸雨的有效措施。开发新能源如氢能、核能等可以从根本上杜绝二氧化硫的产生。至于把烟囱造高,显然不会改变二氧化硫的排放量,对全球酸雨的危害不会减少。在已酸化的土壤中施石灰,是对因酸雨造成的危害的被动治理措施,与从源头上控制二氧化硫的产生无关。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬
燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)=CH4(g)+C2H2 (g)+H2(g) △H1=+156.6 kJ·mol-1
C3H6 (g)=CH4(g)+C2H2 (g ) △H2=+32.4 kJ·mol-1
则相同条件下,反应C3H8(g)= C3H6 (g)+H2(g) 的△H = kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙
烷,电解质是熔融碳酸盐。电池负极反应式为 ;放电时CO32-移向电池的 (填“正”或“负”)极。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素A、B、C、D的原子序数依次递增,它们的核电荷数之和为32,原子最外层电子数之和为10。A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数。则下列叙述正确的是( )
A.B、D的最高价氧化物中,B、D与氧原子形成离子键
B.四种元素的原子半径:A<B<C<D
C.D元素处于元素周期表中第3周期第IV族
D.一定条件下,B单质能置换出D单质,C单质能置换出A单质
查看答案和解析>>
科目:高中化学 来源: 题型:
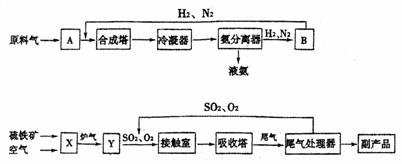
合成氨工业、硫酸工业的生产工艺流程大致为:
合成塔和接触室中的反应分别为:
 |
N2(g)+3H2(g)  2NH3(g) △H﹤0; 2SO2(g)+O2(g)
2NH3(g) △H﹤0; 2SO2(g)+O2(g)  2SO3(g) △H﹤0
2SO3(g) △H﹤0
(1)写出流程中设备的名称:B ,X 。
(2)写出硫铁矿和空气反应的化学方程式
(3)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是 。
(4)采用循环操作可提高原料的利用率,下列生产中,采用循环操作的
是 (填序号)。
①硫酸工业 ②合成氨工业 ③硝酸工业
(5)工业上常用98.3%的浓硫酸吸收SO3而不用稀硫酸或水的原因是 。
(6)工业生产中常用氨——酸法进行尾气脱硫,以达到消除污染、废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在BaCl2溶液中通入SO2气体,未见沉淀生成,若再通入下列四种气体①Cl2 ②NH3 ③NO2 ④H2S均会产生沉淀。
回答下列问题:
(1)通入四种气体时产生的沉淀分别是
①______________________;②______________________;
③______________________;④______________________。
(2)用方程式表示①和④产生沉淀的原因
①________________________________________________________________________;
②________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对某酸性溶液(可能含有Br-、SO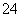 、H2SO3、NH
、H2SO3、NH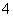 )分别进行如下实验:
)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色;②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;③加入氯水时,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸。
对于下列物质不能确认其在原溶液中是否存在的是 ( )
A.Br- B.SO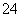
C.H2SO3 D.NH
查看答案和解析>>
科目:高中化学 来源: 题型:
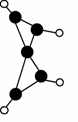
科学家最近在-100℃的低温下合成一种烃X,此分子的模型如右图
(图中的连线表示化学键),下列说法正确的是( )
A.X能使溴的四氯化碳溶液褪色
B.X是一种在常温下能稳定存在的液态烃
C.X分子中在同一平面上的碳原子最多有5个
D.充分燃烧等质量的X和甲烷,X消耗氧气多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com