
| A. | 由①可推测溶液中一定含大量CO32-、S2-、SO32-、NO3- | |
| B. | 由②可推测溶液中一定含大量NO2- | |
| C. | 由③可推测溶液中一定含大量NO3- | |
| D. | 由实验④难以推测溶液中一定含大量SO42- |
分析 ①取少量吸收液于试管中,加入过量的稀盐酸,产生淡黄色浑浊和气体,该黄色沉淀只能是S,将所得的气体依次通入品红溶液、品红褪色,气体含有SO2,通过足量酸性KMnO4溶液,除去SO2,再通过澄清石灰水,石灰水变浑浊,则气体为CO2,故原溶液含有CO32-、S2-、SO32-,酸性条件下S2-、SO32-反应生成S与SO2,不能说明溶液中含有氧化性的离子;
②另取少量待测液于试管中,加入过量的KClO3固体、AgNO3和稀硝酸,有白色沉淀产生,该白色沉淀为AgCl,说明原溶液中含有还原性微粒,据此结合离子的性质分析判断;
③另取少量待测液于试管中,酸化后再加入淀粉KI溶液,呈蓝色,说明有碘单质生成,故原溶液中含有酸性条件有强氧化性的微粒;
④另取少量待测液于试管中,加入足量的BaCl2溶液和稀盐酸,有白色沉淀产生,该白色沉淀为BaSO4,由于溶液中含有SO32-及酸性条件下有氧化性微粒,不能说明原溶液中含有SO42-.
解答 解:A.取少量吸收液于试管中,加入过量的稀盐酸,产生淡黄色浑浊和气体,该黄色沉淀只能是S,将所得的气体依次通入品红溶液、品红褪色,气体含有SO2,通过足量酸性KMnO4溶液,除去SO2,再通过澄清石灰水,石灰水变浑浊,则气体为CO2,故原溶液含有CO32-、S2-、SO32-,酸性条件下S2-、SO32-反应生成S与SO2,不能说明溶液中含有NO3-、NO2-,故A错误;
B.另取少量待测液于试管中,加入过量的KClO3固体、AgNO3和稀硝酸,有白色沉淀产生,该白色沉淀为AgCl,说明原溶液中含有还原性微粒,由于原溶液有S2-、SO32-,不能说明溶液中含有NO2-,故B错误;
C.另取少量待测液于试管中,酸化后再加入淀粉KI溶液,呈蓝色,说明有碘单质生成,故原溶液中含有酸性条件有强氧化性的微粒,故原溶液中可能含有NO3-、NO2- 中的至少1种,故C错误;
D.另取少量待测液于试管中,加入足量的BaCl2溶液和稀盐酸,有白色沉淀产生,该白色沉淀为BaSO4,由于溶液中含有SO32-及酸性条件下有氧化性微粒,可以将SO32-氧化为SO42-,不能说明原溶液中含有SO42-,故D正确;
故选D.
点评 本题考查常见离子的检验方法,为高考高频考点,题目难度中等,注意干扰离子的影响,掌握离子之间发生的反应与现象是关键,试题培养了学生的分析能力及逻辑推理能力.


科目:高中化学 来源: 题型:推断题
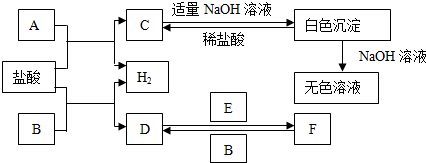
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
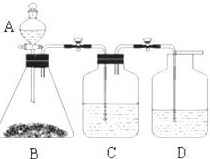 为了确定醋酸溶液、二氧化碳水溶液、苯酚溶液的酸性强弱,有人设计了如图所示的装置进行实验:
为了确定醋酸溶液、二氧化碳水溶液、苯酚溶液的酸性强弱,有人设计了如图所示的装置进行实验:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,正确的是( )
,正确的是( )| A. | 3,3-二甲基-2-乙基戊烷 | B. | 3,3,4-三甲基己烷 | ||
| C. | 2-乙基-3,3-二甲基戊烷 | D. | 3,4,4-三甲基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
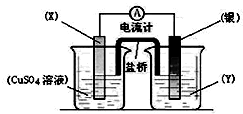 用如图装置实现原电池反应:Cu+2Ag+═Cu2++2Ag
用如图装置实现原电池反应:Cu+2Ag+═Cu2++2Ag查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 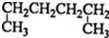 1,4-二甲基丁烷 1,4-二甲基丁烷 | B. | 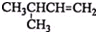 3-甲基丁烯 3-甲基丁烯 | ||
| C. | 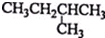 2-甲基丁烷 2-甲基丁烷 | D. | CH2Cl-CH2Cl 二氯乙烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com