
【题目】某有机物含有C、H、O三种元素,其质谱如图所示。将4.3 g该有机物在O2中充分燃烧,使生成物依次通过足量浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重8.8 g,则:

(1)该有机物的摩尔质量为____________g/mol。
(2)该有机物的分子式为 。
(3)1mol该有机物与足量的金属钠反应产生1mol氢气,核磁共振氢谱有两个峰,且面积比为2∶1,请写出其结构简式 。
【答案】(8分)(1) 86(2分) (2) C4H6O2(3分)
(3) ![]() (3分)
(3分)
【解析】
试题分析:(1)根据质荷比可知,该有机物的摩尔质量为86g/mol。
(2)4.3g有机物的物质的量是4.3g÷86g/mol=0.05mol
生成水的质量是2.7g,物质的量是2.7g÷18g/mol=0.15mol
CO2的质量是8.8g,物质的量是8.8g÷44g/mol=0.2mol
所以该有机物分子中碳氢原子的个数分别是4、6个
所以氧原子的个数是![]()
则该有机物的分子式是C4H6O2
(3)1mol该有机物与足量的金属钠反应产生1mol氢气,石墨含有2个羟基。核磁共振氢谱有两个峰,且面积比为2∶1,则该有机物的结构简式是![]() 。
。


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.按系统命名法,![]() 的名称为2,7,7-三甲基-3-乙基辛烷
的名称为2,7,7-三甲基-3-乙基辛烷
B.实验证实![]() 可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键
可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键
C. DDT的结构简式为 ,分子中最多有14个碳原子共平面
,分子中最多有14个碳原子共平面
D.  的单体是CH3-C≡C-CH3和CH2=CH-CN
的单体是CH3-C≡C-CH3和CH2=CH-CN
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是
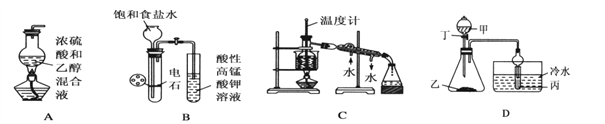
A. 实验室制乙烯
B. 实验室制乙炔并验证乙炔能发生氧化反应
C. 实验室中分馏石油
D. 若甲为硫酸,乙为贝壳(粉状),丙为苯酚钠溶液,验证硫酸、碳酸、苯酚酸性的强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.92gCu投入一定量的浓HNO3溶液中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下的气体672mL,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的氧气,恰好使气体完全溶于水,则通入的氧气的体积为( )
A. 504mL B. 224 mL C. 336 mL D. 168 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.1000 mol/L KOH溶液滴定20.00 mL 0.1000 mol/L CH3COOH溶液,滴定中pH变化如图,下列关系错误的是

A.V=0.00mL时,CH3COOH溶液pH=3,其电离平衡常数K≈10-5mol/L
B.V=10.00mL时,溶液中2c(K+)=c(CH3COO-)+c(CH3COOH)
C.V≥20.00mL时,溶液中一定有c(K+)>c(CH3COO-)>c(OH-)> c(H+)
D.溶液pH=7时,![]() =1
=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,NOx和SO2是雾霾的主要成分。
Ⅰ.NOx主要来源于汽车尾气。
已知:N2(g) + 2O2(g)![]() 2NO2(g) ΔH=+67.5kJ/mol
2NO2(g) ΔH=+67.5kJ/mol
2CO(g) + O2(g)![]() 2CO2(g) ΔH=-566.00kJ/mol。
2CO2(g) ΔH=-566.00kJ/mol。
(1)为了减轻大气污染,在汽车尾气排气管口采用催化剂将NO2和CO转化成无污染气体参与大气循环。写出该反应的热化学方程式 。
(2)T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中发生反应2NO(g)+2CO(g)![]() 2CO2(g) +N2(g),保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化的关系如图所示。
2CO2(g) +N2(g),保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化的关系如图所示。


①下列能说明该反应达到平衡状态的是____________。
A.体系压强保持不变 B.NO和CO的转化率相等
C.混合气体的密度保持不变 D.混合气体的平均相对分子质量保持不变
②前10min以N2表示的化学反应速率v(N2)=_______________;T℃时该化学反应的平衡常数K=_______________;平衡时若保持温度不变,再向容器中充入CO、N2各0.8mol,平衡将_______移动(填“向左”、“向右”或“不)。15min时,若降低温度,导致n(NO)发生如图所示的变化,则该反应的ΔH 0(填“>”、“=”或“<”)。
Ⅱ.SO2主要来源于煤的燃烧。燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关键。
(3)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。
物质A的化学式为_____________,阴极的电极反应式是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com