


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
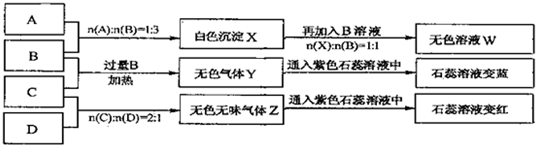
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol羟基(-OH)中含有的质子数为10 NA |
| B、相同状况下,22.4 L NO和11.2 L O2反应,生成物含有NA个分子 |
| C、在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2 NA个电子 |
| D、1 mol Na2O2含有2 NA个阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
| B、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液不一定是钠盐溶液 |
| C、向某未知溶液中加入稀NaOH溶液,将湿润的红色石蕊试纸靠近试管口,无明显现象,则原溶液中没有NH4+ |
| D、某溶液中加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定含有CO32- |
| B、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定含有Na+ |
| C、向某溶液中滴加BaCl2溶液产生白色沉淀,再滴加稀HNO3沉淀不溶解,则原溶液中一定含有SO42- |
| D、向某溶液中滴加KSCN 溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O2- 1s22s22p4 |
| B、Ca[Ar]3d2 |
| C、Si 1s22s22p63s23p2 |
| D、Zn[Ar]3d104s1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、处于最低能量的原子叫做基态原子 |
| B、4f 4表示4f能级有四个轨道 |
| C、同一原子中,2p、3d、4f能级的轨道数依次增多 |
| D、同一原子中,2p、3p、4p电子的能量逐渐增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com