
【题目】取等物质的量浓度的NaOH溶液两份A和B,每份100mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸体积之间的关系如图所示。下列说法正确的是
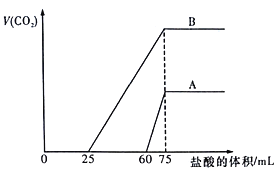
A. B曲线中消耗盐酸0<V(HCl)<25mL时发生的离子反应为: OH-+H+=H2O,H++CO32-=HCO3-
B. 原NaOH溶液的物质的量浓度为0.75mol/L
C. B曲线最终产生的CO2体积(标准状况下)为112mL
D. 加盐酸之前A溶液中的溶质是碳酸钠和碳酸氢钠
【答案】C
【解析】A、当生成CO2气体时,发生反应HCO3-+H+=H2O+CO2↑,对于B溶液来说,滴加盐酸25mL时没有气体生成。假设原溶液中只有碳酸钠,生成碳酸氢钠需要盐酸的体积和碳酸氢钠生成氯化钠需要盐酸的体积相等,实际上需要盐酸的体积小于碳酸氢钠生成氯化钠需要盐酸的体积,说明原溶液中的溶质是碳酸钠和碳酸氢钠,所以B曲线中消耗盐酸0<v(HCl)<25mL时发生的离子反应为:H++CO32-=HCO3-,故A错误;B、先向氢氧化钠溶液中通入二氧化碳,后向通入二氧化碳的氢氧化钠溶液中滴加盐酸,当二氧化碳气体完全放出时,溶液的溶质是氯化钠,该反应的实质是盐酸和氢氧化钠反应生成氯化钠,盐酸和氢氧化钠反应的物质的量之比为1:1,设氢氧化钠的物质的量浓度为cmol/L,0.1L×cmol/L=0.1mol/L×0.075L,c=0.075,故B错误;C、通过C知,B溶液中的溶质是碳酸钠和碳酸氢钠,碳酸钠和盐酸反应生成碳酸氢钠,有气体生成的化学反应方程式为:HCO3-+H+=H2O+CO2↑,所以当盐酸的为25mL时有二氧化碳生成,即发生的化学反应为:HCO3-+H+=H2O+CO2↑,生成的二氧化碳的物质的量= n(H+)=0.1mol/L×(0.075L-0.025L)=0.005mol,则二氧化碳的体积=0.005mol ×22.4L/mol =0.112L=112mL,故C正确;D、当生成CO2气体时,发生反应HCO3-+H+=H2O+CO2↑,对于A溶液来说,滴加盐酸60mL时没有气体生成,可能发生OH-+H+=H2O和CO32-+H+=HCO3-,假设原溶液中只有碳酸钠,生成碳酸氢钠需要盐酸的体积和碳酸氢钠生成氯化钠需要盐酸的体积相等,实际上需要盐酸的体积远远大于碳酸氢钠生成氯化钠需要盐酸的体积,说明原溶液中的溶质是氢氧化钠和碳酸钠,故D错误;故选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】胶体区别于其它分散系的特征是( )
A.胶体粒子直径在1nm~100nm之间B.胶体粒子带电荷
C.胶体粒子不能穿过半透膜D.胶体粒子能够发生布朗运动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式不正确的是( )
A.焊接铁轨:2Fe+Al2O3 ![]() 2Al+Fe2O3
2Al+Fe2O3
B.工业固氮:N2+3H2 ![]() 2NH3
2NH3
C.用纯碱除油污:CO32﹣+H2OHCO3﹣+OH﹣
D.用湿润的淀粉KI试纸检验Cl2:Cl2+2I﹣═2Cl﹣+I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气设计了如下实验装置。
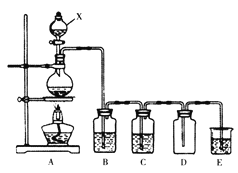
请按要求回答下列问题:
(1)仪器X的名称为_________________。
(2)已知装置B中选用的试剂为饱和食盐水,其作用为___________________。
(3)将氯气通入紫色石蕊试液C中可以观察到的现象是________________________。
(4)装置E中装有NaOH溶液,该装置中反应的化学方程式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有如下合成路线,甲经二步转化为丙: 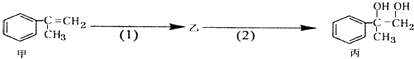
下列叙述错误的是( )
A.甲和丙均可与酸性KMnO4溶液发生反应
B.反应(1)的无机试剂是液溴,铁作催化剂
C.步骤(2)产物中可能含有未反应的甲,可用溴水检验是否含甲
D.反应(2)反应属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,某有机物和过量Na反应得到V1 L氢气,另一份等量的该有机物和足量的NaHCO3反应得到V2 L二氧化碳,若V1=V2≠0,则该有机物可能是( )
A.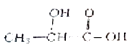
B.HOOC﹣COOH
C.HOCH2CH2OH
D.CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如右图所示。下列分析不正确的是( )

A. ①代表滴加H2SO4溶液的变化曲线
B. b点,溶液中大量存在的离子是Na+、OH–
C. c点,两溶液中含有相同量的OH–
D. a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在冶金工业上,均不能用常见化学还原剂制得的金属组是( )
A.Na、Ba、Mg、Al
B.Na、K,Zn、Fe
C.Zn、Fe、Cu、Ag
D.Mg、Al、Zn、Fe
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com