

| A. | 实验Ⅰ:液体分层,下层呈无色 | |
| B. | 实验Ⅱ:烧杯中先出现白色沉淀,后溶解 | |
| C. | 实验Ⅲ:试管中溶液颜色先变为灰绿色后迅速变为红色 | |
| D. | 实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
分析 A.四氯化碳密度比水大;
B.氢氧化铝不溶于弱碱;
C.溶液呈血红色,而不是沉淀;
D.根据CaO吸水并放热分析.
解答 解:A.碘易溶于四氯化碳且四氯化碳密度比水大,色层在下层,故A错误;
B.氯化铵和氢氧化钙反应生成氨气,氨气溶于水呈碱性,与氯化铝反应生成氢氧化铝沉淀,氢氧化铝不溶于弱碱,故B错误;
C.氯化铁与KSCN反应生成Fe(SCN)3,溶液呈红色,而不是生成沉淀,故C错误;
D.CaO吸水生成氢氧化钙,饱和CuSO4溶液中水减少,会析出蓝色晶体,故D正确.
故选D.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大,易错点为B,注意两性氢氧化物的性质.


科目:高中化学 来源: 题型:选择题
| A. | 1 mol Na被完全氧化生成Na2O2,失去2NA个电子 | |
| B. | 常温常压下,18 g H2O 中含有的原子总数为3NA | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA | |
| D. | 1 mol Cl2与1 mol Fe反应,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
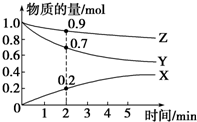 某温度时,在2L容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.由此分析,该反应的化学方程式为3Y+Z?2X;从反应开始至2min时,Z的反应速率为0.025mol•L-1•min-1.
某温度时,在2L容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.由此分析,该反应的化学方程式为3Y+Z?2X;从反应开始至2min时,Z的反应速率为0.025mol•L-1•min-1.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | X:3s23P1 Y:3s23P5 | B. | X:2s22P3 Y:2s22P4 | ||
| C. | X:3s23P1 Y:3s23P4 | D. | X:3s2 Y:2s22P3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 离子 | Na+ | Al3+ | Cl- | X |
| 个数 | 2a | a | a | b |
| A. | NO3-、2a | B. | SO42-、2a | C. | OH-、2a | D. | SO42-、4a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
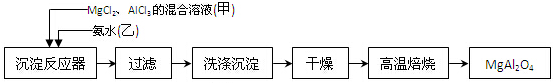
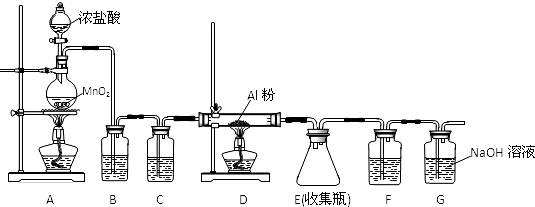
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2互为同分异构体.请填空:
,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2互为同分异构体.请填空: +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$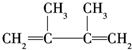 +2NaBr+2H2O;
+2NaBr+2H2O; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
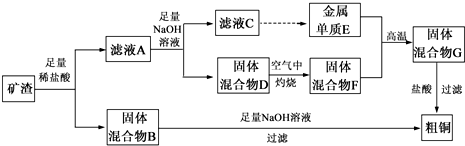
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ②③ | C. | ①④ | D. | ①③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com