

 ,该分子的核磁共振氢谱中有两组峰,其峰面积之比是3:2,故C错误;
,该分子的核磁共振氢谱中有两组峰,其峰面积之比是3:2,故C错误;

 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
| A、除去石英中混有的少量铝粉,可加入氢氧化钠溶液溶解后过滤 |
| B、向含有少量FeBr2的FeCl2溶液中,加入适量氯水,再加CCl4萃取分液,以除去FeCl2溶液中的FeBr2 |
| C、除去乙酸乙酯中混有的少量乙酸,加入饱和氢氧化钠溶液振荡后分液 |
| D、已知:Ksp(CuS)<Ksp(FeS),可加入过量的难溶电解质FeS,使水中少量的Cu2+转化成硫化物沉淀而除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:
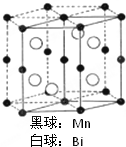 磁光盘机(Magnetic Optical Disk Drive,MO)是一种可重写的光盘驱动器,它使用磁光盘片作存储媒体.磁光存储的研究是Williams等在1957年使Mn和Bi形成的晶体薄膜磁化并用光读取之后开始的.如图是该物质的晶体结构,其化学式可表示为( )
磁光盘机(Magnetic Optical Disk Drive,MO)是一种可重写的光盘驱动器,它使用磁光盘片作存储媒体.磁光存储的研究是Williams等在1957年使Mn和Bi形成的晶体薄膜磁化并用光读取之后开始的.如图是该物质的晶体结构,其化学式可表示为( )| A、Mn2Bi |
| B、MnBi |
| C、MnBi3 |
| D、Mn4Bi3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、1:1 | B、1:2 |
| C、1:3 | D、1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
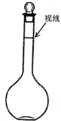 实验室需用230mL 0.1mol/L的Na2CO3溶液,填空并回答下列问题:
实验室需用230mL 0.1mol/L的Na2CO3溶液,填空并回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com