
���� ��������ʽ�������ֵ����ʵ����ı仯����ƽ��ʱ����ֵ����ʵ�����
��1�����ݷ���ʽ����A�����ʵ����ɼ���A��Ũ�ȣ�����ת����=$\frac{��ת�������ʵ���}{��ʼ���ʵ���}$��100%���㣬����v=$\frac{��c}{��t}$���㷴Ӧ���ʣ�
��2����ѧƽ�ⳣ�������������Ũ����֮�����Է�Ӧ���Ũ����֮��������ƽ�ⳣ���ı仯���ж��¶ȶ�ƽ���ƶ���Ӱ�죻
��3���÷�Ӧ��Ӧǰ������������䣬����ѹǿƽ�ⲻ�ƶ����ݴ��ж�A��ת���ʣ�
��� �⣺���ڷ�Ӧ 3A��g��+B��g�� 2C��g��+2D��g����
2C��g��+2D��g����
��ʼ��mol����2 2 0 0
�仯��mol����1.2 0.4 0.8 0.8
ƽ�⣨mol����0.8 1.6 0.8 0.8
��1�������������֪��ƽ��ʱA�����ʵ���Ϊ0.8mol������B��ƽ��Ũ��Ϊc��A��=$\frac{0.8mol}{2L}$=0.4mol/L��
B��ת����Ϊ$\frac{0.4mol}{2mol}$��100=20%��
ƽ��ʱD�����ʵ���Ϊ0.8mol��������D��ʾ��ƽ����Ӧ����Ϊv��D��=$\frac{\frac{0.8mol}{2L}}{2min}$=0.2mol/��L•min����
�ʴ�Ϊ��0.4mol/L��20%��0.2mol/��L•min����
��2����ѧƽ�ⳣ�������������Ũ����֮�����Է�Ӧ���Ũ����֮������K1=$\frac{c{\;}^{2}��C����c{\;}^{2}��D��}{c{\;}^{3}��A����c��B��}$=$\frac{��\frac{0.8mol}{2L}��^{2}•��\frac{0.8mol}{2L}��^{2}}{��{\frac{0.8mol}{2L}��}^{3}•��\frac{1.6mol}{2L}��}$=0.5��K2=l������K300����K350����˵�������¶�ƽ��������Ӧ�����ƶ���������Ӧ���ȣ���H��0��
�ʴ�Ϊ��$\frac{c{\;}^{2}��C����c{\;}^{2}��D��}{c{\;}^{3}��A����c��B��}$��0.5������
��3���ɷ���ʽ��֪������Ļ�ѧ������֮��ǰ����ȣ���Ӧǰ������������䣬ѹǿ��ƽ����Ӱ�죬��С�����ݻ�����A��ת���ʲ��䣬
�ʴ�Ϊ�����䣻��Ӧǰ������������䣬ѹǿ��ƽ����Ӱ�죮
���� ���⿼�鷴Ӧ���ʵļ��㡢��Чƽ��ȣ��Ѷ��еȣ�ע������ʽ���ⷨ�����ã�ע����յ�Чƽ��������Ӧ�ã�


 �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д� ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д� ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д� ��У���һ��ͨϵ�д�
��У���һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | V��NO2����V��O2��=2��1 | B�� | V��NO����V��O2��=2��1 | ||
| C�� | V��NH3����V��O2��=2��1 | D�� | V��NO2����V��NO����V��O2��=1��1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��Cu2+��NO${\;}_{3}^{-}$��SO${\;}_{4}^{2-}$ | B�� | H+��K+��HCO${\;}_{3}^{-}$��Ca2+ | ||
| C�� | Ba2+��Mg2+��OH-��Cl- | D�� | Fe3+��NH${\;}_{4}^{+}$��S2-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
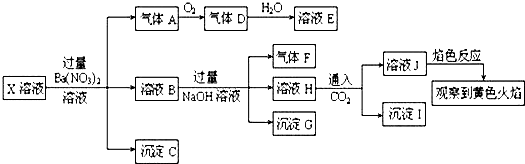
| A�� | X�в���ȷ����������Fe3+��A13+��K+��Na+��C1- | |
| B�� | ����G�м��������ܽ⣬�μ�KSCN��Һ�Ժ�ɫ������ȷ��ԭ��Һ����Fe3+ | |
| C�� | ��ҺJ��ɫ��Ӧ�Ի�ɫ����˵��ԭ��Һ�д���Na+ | |
| D�� | ����Iһ����A1��OH��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���ữѧʽ | CH3COOH | HCLO | H2CO3 |
| ����ƽ�ⳣ����25�棩 | 1.75��10-5 | 3.0��10-8 | K1=4.4��10-7 K2=4.7��10-11 |
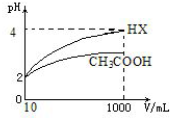
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 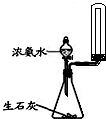 �Ʊ��������� | B�� | 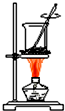 �������ճɻ� | ||
| C�� | 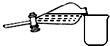 ��Һʱȡ���²�Һ�� | D�� | 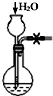 ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
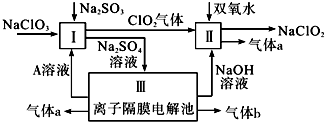
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ͬ�������£����ױȺ����ȶ� | |
| B�� | ������������ȼ�������� | |
| C�� | ���Ͱ��Ľṹ��ͬ | |
| D�� | ������ͬ�������£����ױȰ����ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com