
(10分) 在食品加工领域,应用二氧化硫的最主要原因是避免氧化和防腐。在我国葡萄酒中二氧化硫的最大使用量为0.2500g/kg,二氧化硫残留量不得超过0.05000g/kg。葡萄酒中的二氧化硫包括游离的和结合的,因而加人氢氧化钾使之破坏其结合状态,并使之固定S02+2KOH ==K2S03+H20;然后加入硫酸又使二氧化硫游离,K2S03+H2S04 == K2S04+H2O+S02↑;加入过量的I2氧化S02;过量的I2可用硫代硫酸钠进行滴定,I2+2Na2S203== Na2S406+2NaI。
以下是某实验小组测定某品牌的干白葡萄酒(密度为1.12g/ml)中二氧化硫的含量是否超标的实验方案。
实验步骤:
①用移液管量取50.00ml样品于250ml锥形瓶中,加入25.00 ml1mol/L氢氧化钾溶液,加塞,摇匀;
②静置15min;
③打开塞子,加入25.00ml1:3硫酸溶液使溶液呈酸性,再加入25.00ml0.01000mol/L碘溶液,迅速的加塞,摇匀;
④用 滴定管移取步骤③中溶液25.00ml,加入适量0.1%的A溶液作指示剂,立即用浓度为0.002000mol/L的硫代硫酸钠溶液滴定,并记录消耗硫代硫酸钠溶液的体积;
⑤重复以上实验2次;
⑥数据处理,得出结论。
请回答下列问题:
(1)以上实验方案中步骤③中加碘溶液时发生的离子反应方程式是: ;
(2)步骤①-③中始终要将锥形瓶加塞进行操作的原因是 ;
(3)步骤④的A溶液最合适的是 ;滴定终点的判断方法是 ;
(4)步骤④应该选用 (填空“酸式”或“碱式”)滴定管;
(5)该小组三次实验消耗的Na2S203溶液的体积数据记录如下:
| 序号 | 滴定前/mL | 滴定后/mL |
| ① | 1.35 | 19.40 |
| ② | 1.05 | 19.00 |
| ③ | 1.58 | 20.91 |
根据数据计算该样品中总二氧化硫的浓度为 mol/L,故该干白葡萄酒是 (填“合格”“不合格”)产品。
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源:2013届陕西省东方中学新高三开学适应性测试化学试卷(带解析) 题型:填空题
(10分)维生素C(分子式为C6H8O6)又名抗坏血酸,可预防感染、坏血病等,也是一种常见的食品添加剂,能够阻止空气中的氧气将食品氧化变质。维生素C具有酸性和强还原性,其工业合成路线如下图所示: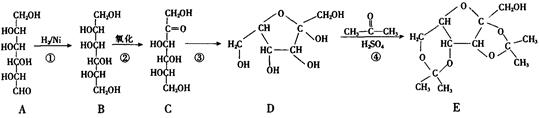

(1)上述合成过程中与A互为同分异构体的有 (填写字母代号)。
(2)上述反应中,属于加成反应的有 (填数字序号)。
(3)反应④除生成E外,还有 生成。比较D和C的结构可知,C可看成由D通过反应⑤氧化得到,在工业生产中设计④和⑥两步的目的是
。
(4)维生素C的结构简式是 。
查看答案和解析>>
科目:高中化学 来源:2012届浙江省富阳市新登中学高三上学期期中考试化学试卷 题型:实验题
(10分)在食品加工领域,应用二氧化硫的最主要原因是避免氧化和防腐。在我国葡萄酒中二氧化硫的最大使用量为0.2500g/kg,二氧化硫残留量不得超过0.05000g/kg。葡萄酒中的二氧化硫包括游离的和结合的,因而加人氢氧化钾使之破坏其结合状态,并使之固定S02+2KOH ="=" K2S03+H20;然后加入硫酸又使二氧化硫游离,K2S03+H2S04 ="=" K2S04+H2O+S02↑;加入过量的I2氧化S02;过量的I2可用硫代硫酸钠进行滴定,I2+2Na2S203="=" Na2S406+ 2NaI。
以下是某实验小组测定某品牌的干白葡萄酒(密度为1.12g/ml)中二氧化硫的含量是否超标的实验方案。
实验步骤:
①用移液管量取50.00ml样品于250ml锥形瓶中,加入25.00 ml1mol/L氢氧化钾溶液,加塞,摇匀;
②静置15min;
③打开塞子,加入25.00ml1:3硫酸溶液使溶液呈酸性,再加入25.00ml0.01000mol/L碘溶液,迅速的加塞,摇匀;
④用 滴定管移取步骤 ③中溶液25.00ml,加入适量0.1%的A溶液作指示剂,立即用浓度为0.002000mol/L的硫代硫酸钠溶液滴定,并记录消耗硫代硫酸钠溶液的体积;
③中溶液25.00ml,加入适量0.1%的A溶液作指示剂,立即用浓度为0.002000mol/L的硫代硫酸钠溶液滴定,并记录消耗硫代硫酸钠溶液的体积;
⑤重复以上实验2次;
⑥数据处理,得出结论。
请回答下列问题:
(1)以上实验方案中步骤③中加碘溶液时发生的离子反应方程式是: ;
(2)步骤①-③中始终要将锥形瓶加塞进行操作的原因是 ;
(3)步骤④的A溶液最合适的是 ;滴定终点的判断方法是 ;
(4)步骤④应该选用 (填空“酸式”或“碱式”)滴定管;
(5)该小组三次实验消耗的Na2S203溶液的体积数据记录如下:
| 序号 | 滴定前/mL | 滴定后/mL |
| ① | 1.35 | 19.40 |
| ② | 1.05 | 19.00 |
| ③ | 1.58 | 20. 91 91 |
查看答案和解析>>
科目:高中化学 来源:2014届云南省高二上学期期末考试化学试卷(解析版) 题型:填空题
(每空2分,共10分)食品安全关系国计民生,影响食品安全的因素很多。
(1)聚偏二氯乙烯( )具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。
)具有超强阻隔性能,可作为保鲜食品的包装材料。它是由________(写结构简式)发生加聚反应生成的。
(2)劣质植物油中的亚油酸[CH3(CH2)4—CH===CH—CH2—CH===CH—(CH2)7COOH]含量很低。下列关于亚油酸的说法中,正确的是________。
A.分子式为C18H34O2
B.一定条件下能与乙酸发生酯化反应
C.能和NaOH溶液反应
D.能使酸性KMnO4溶液褪色
(3)假酒中甲醇(CH3OH)含量超标,请写出Na和甲醇反应的化学方程式:____________________。
(4)劣质奶粉中蛋白质含量很低。蛋白质水解的最终产物是__________________。
(5)在淀粉中加入吊白块制得的粉丝有毒。淀粉最终的水解产物是葡萄糖。请设计实验证明淀粉已经全部水解,写出操作、现象和结论:_________________________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省富阳市高三上学期期中考试化学试卷 题型:实验题
(10分) 在食品加工领域,应用二氧化硫的最主要原因是避免氧化和防腐。在我国葡萄酒中二氧化硫的最大使用量为0.2500g/kg,二氧化硫残留量不得超过0.05000g/kg。葡萄酒中的二氧化硫包括游离的和结合的,因而加人氢氧化钾使之破坏其结合状态,并使之固定S02+2KOH == K2S03+H20;然后加入硫酸又使二氧化硫游离,K2S03+H2S04 == K2S04+H2O+S02↑;加入过量的I2氧化S02;过量的I2可用硫代硫酸钠进行滴定,I2+2Na2S203== Na2S406+ 2NaI。
以下是某实验小组测定某品牌的干白葡萄酒(密度为1.12g/ml)中二氧化硫的含量是否超标的实验方案。
实验步骤:
①用移液管量取50.00ml样品于250ml锥形瓶中,加入25.00 ml1mol/L氢氧化钾溶液,加塞,摇匀;
②静置15min;
③打开塞子,加入25.00ml1:3硫酸溶液使溶液呈酸性,再加入25.00ml0.01000mol/L碘溶液,迅速的加塞,摇匀;
④用 滴定管移取步骤③中溶液25.00ml,加入适量0.1%的A溶液作指示剂,立即用浓度为0.002000mol/L的硫代硫酸钠溶液滴定,并记录消耗硫代硫酸钠溶液的体积;
⑤重复以上实验2次;
⑥数据处理,得出结论。
请回答下列问题:
(1)以上实验方案中步骤③中加碘溶液时发生的离子反应方程式是: ;
(2)步骤①-③中始终要将锥形瓶加塞进行操作的原因是 ;
(3)步骤④的A溶液最合适的是 ;滴定终点的判断方法是 ;
(4)步骤④应该选用 (填空“酸式”或“碱式”)滴定管;
(5)该小组三次实验消耗的Na2S203溶液的体积数据记录如下:
|
序号 |
滴定前/mL |
滴定后/mL |
|
① |
1.35 |
19.40 |
|
② |
1.05 |
19.00 |
|
③ |
1.58 |
20.91 |
根据数据计算该样品中总二氧化硫的浓度为 mol/L,故该干白葡萄酒是 (填“合格”“不合格”)产品。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com