
ЁОЬтФПЁПЮЊСЫЗРжЙЕЊбѕЛЏЮяЖдПеЦјЕФЮлШОЃЌШЫУЧВЩШЁСЫКмЖрДыЪЉЁЃ
ЃЈ1ЃЉШчгУCH4ДпЛЏЛЙдNO2ПЩвдЯћГ§ЕЊбѕЛЏЮяЕФЮлШОЃЌЗЂЩњЕФЗДгІШчЯТЃК CH4(g)+2NO2(g)![]() N2(g)ЃЋCO2(g)+2H2O(g) ЁїHЃНЃ867 kJЁЄmolЃ1ЁЃ
N2(g)ЃЋCO2(g)+2H2O(g) ЁїHЃНЃ867 kJЁЄmolЃ1ЁЃ
ЂйЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ_________ЁЃ
AЃЎдкШнЦїжаГфШы1mol CH4КЭ2 mol NO2ЃЌЕБЬхЯЕжаn(CH4)/n(NO2)БШжЕВЛЫцЪБМфБфЛЏЪБЃЌЗДгІДяЕНЦНКтзДЬЌ
BЃЎКуЮТКуШнЪБЃЌЕБЛьКЯЦјЬхЕФУмЖШВЛЫцЪБМфБфЛЏЪБЃЌИУЗДгІДяЕНЦНКтзДЬЌ
CЃЎЬхЯЕДяЕНЦНКтКѓЃЌЩ§ИпЮТЖШЃЌЬхЯЕжаЕФЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПдіДѓ
DЃЎКуЮТКубЙЪБЃЌГфШыCH4гаРћгкЬсИпЕЊбѕЛЏЮяЕФзЊЛЏТЪ
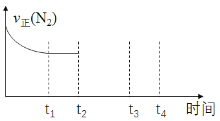
Ђкдкt2ЪБПЬЃЌНЋШнЦїЕФШнЛ§бИЫйРЉДѓЕНдРДЕФ2БЖЃЌдкЦфЫћЬѕМўВЛБфЕФЧщПіЯТЃЌt3ЪБПЬДяЕНаТЕФЦНКтзДЬЌЁЃЧыдкгвЭМжаВЙГфЛГіДгt2ЕНt4ЪБПЬvе§(N2) ЫцЪБМфЕФБфЛЏЧњЯпЃК____________
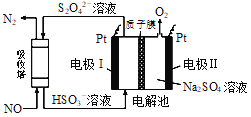
ЃЈ2ЃЉЯжгаЕФЦћГЕЮВЦјДІРэЕФдРэЪЧЃКNO(g)+2CO(g)![]() N2(g) +2CO2(g)ЃЌЭЈГЃЪЙКЌЪЪЕББШР§ЕФNOЁЂCOЮВЦјЭЈЙ§зАгаИпаЇДпЛЏМСЕФДІРэзАжУЁЃЧыИљОнвдЯТЯрЙиЪ§ОнЃЌЗжЮіНіЪЙгУДпЛЏМСФмЗёгааЇЯћГ§NOЁЂCOЮВЦјЮлШО___________ЁЃ
N2(g) +2CO2(g)ЃЌЭЈГЃЪЙКЌЪЪЕББШР§ЕФNOЁЂCOЮВЦјЭЈЙ§зАгаИпаЇДпЛЏМСЕФДІРэзАжУЁЃЧыИљОнвдЯТЯрЙиЪ§ОнЃЌЗжЮіНіЪЙгУДпЛЏМСФмЗёгааЇЯћГ§NOЁЂCOЮВЦјЮлШО___________ЁЃ
ЗДгІ | 25ЁцЪБЕФЦНКтГЃЪ§ | ьЪБф |
ЗДгІIЃК2NO(g) | K1=1ЁС1030 | ЁїH=Ѓ180.5kJ/mol |
ЗДгІIIЃК2CO2 (g) | K2=4ЁС10Ѓ92 | ЁїH= +566.0kJ/mol |
ЃЈ3ЃЉгУNH3ДпЛЏЛЙдNOxвВПЩвдЯћГ§ЕЊбѕЛЏЮяЕФЮлШОЃЌЦфЗДгІдРэЮЊЃКNO(g) +NO2(g)+2NH3(g)![]() 2N2(g) + 3H2O(g)ЁЃвЛЖЈЮТЖШЯТЃЌдкФГКуЖЈбЙЧПЮЊPЕФУмБеШнЦїжаГфШывЛЖЈСПЕФNOЁЂNO2КЭNH3ЃЌДяЕНЦНКтзДЬЌКѓЃЌШнЦїжаКЌn(NO)=a molЃЌn(NO2)=2a molЃЌn(NH3)=2a molЃЌn(N2)=2b molЃЌЧвN2(g)ЕФЬхЛ§ЗжЪ§ЮЊ1/3ЃЌЧыМЦЫуДЫЪБЕФЦНКтГЃЪ§Kp=________________ЁЃЃЈгУжЛКЌPЕФЪНзгБэЪОЃЌЧвЛЏжСзюМђЪНЃЉЁЃЃЈБИзЂЃКЖдгкгаЦјЬхВЮМгЕФЗДгІЃЌПЩгУФГзщЗжЕФЦНКтЗжбЙДњЬцЮяжЪЕФСПХЈЖШМЦЫуЦНКтГЃЪ§ЃЌМЧзїKPЁЃШчp(NO2)ЮЊNO2ЕФЦНКтЗжбЙЃЌp(NO2)=x(NO2)pЃЌpЮЊЦНКтзмбЙЃЌx(NO2)ЮЊЦНКтЬхЯЕжаNO2ЕФЮяжЪЕФСПЗжЪ§ЁЃЃЉ
2N2(g) + 3H2O(g)ЁЃвЛЖЈЮТЖШЯТЃЌдкФГКуЖЈбЙЧПЮЊPЕФУмБеШнЦїжаГфШывЛЖЈСПЕФNOЁЂNO2КЭNH3ЃЌДяЕНЦНКтзДЬЌКѓЃЌШнЦїжаКЌn(NO)=a molЃЌn(NO2)=2a molЃЌn(NH3)=2a molЃЌn(N2)=2b molЃЌЧвN2(g)ЕФЬхЛ§ЗжЪ§ЮЊ1/3ЃЌЧыМЦЫуДЫЪБЕФЦНКтГЃЪ§Kp=________________ЁЃЃЈгУжЛКЌPЕФЪНзгБэЪОЃЌЧвЛЏжСзюМђЪНЃЉЁЃЃЈБИзЂЃКЖдгкгаЦјЬхВЮМгЕФЗДгІЃЌПЩгУФГзщЗжЕФЦНКтЗжбЙДњЬцЮяжЪЕФСПХЈЖШМЦЫуЦНКтГЃЪ§ЃЌМЧзїKPЁЃШчp(NO2)ЮЊNO2ЕФЦНКтЗжбЙЃЌp(NO2)=x(NO2)pЃЌpЮЊЦНКтзмбЙЃЌx(NO2)ЮЊЦНКтЬхЯЕжаNO2ЕФЮяжЪЕФСПЗжЪ§ЁЃЃЉ
ЃЈ4ЃЉгУМфНгЕчЛЏбЇЗЈЖдДѓЦјЮлШОЮяNOНјааЮоКІЛЏДІРэЃЌЦфдРэЪОвтШчЭМЃЈжЪзгФЄдЪаэH+КЭH2OЭЈЙ§ЃЉЃЌЕчМЋIЗЂЩњЕФЕчМЋЗДгІЮЊ_________________________ЁЃ
ЁОД№АИЁПCD 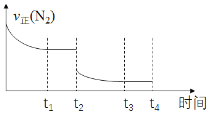 гЩЗДгІIКЭIIЕФЦНКтГЃЪ§ЃЌПЩжЊ2NO(g)+2CO(g)
гЩЗДгІIКЭIIЕФЦНКтГЃЪ§ЃЌПЩжЊ2NO(g)+2CO(g)![]() N2(g) +2CO2(g)ЕФK= K1/K2ЃН2.5ЁС10121ЃЌИУЗДгІЯђе§ЗНЯђЕФЧїЪЦКмДѓЃЌЪЙгУКЯЪЪЕФДпЛЏМСМгПьЗДгІЫйТЪЃЌЛљБОЩЯПЩвдГ§ШЅЮлШОЦјЬх 5625P/4 2HSO3Ѓ + 2eЃ+ 2H+ = S2O42Ѓ+2H2O
N2(g) +2CO2(g)ЕФK= K1/K2ЃН2.5ЁС10121ЃЌИУЗДгІЯђе§ЗНЯђЕФЧїЪЦКмДѓЃЌЪЙгУКЯЪЪЕФДпЛЏМСМгПьЗДгІЫйТЪЃЌЛљБОЩЯПЩвдГ§ШЅЮлШОЦјЬх 5625P/4 2HSO3Ѓ + 2eЃ+ 2H+ = S2O42Ѓ+2H2O
ЁОНтЮіЁП
ЃЈ1ЃЉЂйИљОнДяЕНЦНКтзДЬЌЪБЃЌе§ЗДгІЫйТЪЕШгкФцЗДгІЫйТЪЃЛЛьКЯЮяжаИїзщЗжЕФАйЗжКЌСПБЃГжВЛБфвдМАЯрЙиЕФСПВЛБфРДЗжЮіХаЖЯЃЛ
Ђкt2ЪБШнЛ§РЉДѓЕНдРДЕФ2БЖЃЌзщЗжХЈЖШМѕаЁЃЌИљОнРеЯФЬиСадРэЃЌЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЃЌvе§(N2)МѕаЁЃЌt3ЪБДяЕНЦНКтЃЌвдДЫЛГіЭМЯёЃЛ
ЃЈ2ЃЉИљОнвдЩЯгаЙиЪ§ОнЃЌПЩОнИЧЫЙЖЈТЩЗжЮіЃЌNOгыCOЗДгІЕФKжЕДѓаЁЃЌНјЖјНтД№ЃЛ
ЃЈ3ЃЉЯШИљОнN2(g)ЕФЬхЛ§ЗжЪ§ЮЊ1/3ЃЌЧѓГіИїзщЗнЕФЮяжЪЕФСПЗжЪ§ЃЌдйИљОн
Kp=![]() МЦЫуЦНКтГЃЪ§ЃЛ
МЦЫуЦНКтГЃЪ§ЃЛ
ЃЈ4ЃЉЕчМЋIЮЊвѕМЋЃЌвѕМЋЩЯЪЧHSO3ЃЛёЕУЕчзгЩњГЩS2O42ЃЃЌдкЫсадЬѕМўЯТЛЙЩњГЩЫЎЃЌНсКЯЕчзгЪиКуЁЂЕчКЩЪиКуаДГіЕчМЋЗДгІЪНЁЃ
ЃЈ1ЃЉЂйAЃЎгЩЗДгІЪНКЭЦ№ЪММгСЯСППЩжЊЃЌЬхЯЕжаn(CH4)/n(NO2)БШжЕЪМжеВЛБфЃЌВЛФмзїЮЊДяЕНЦНКтзДЬЌЕФБъжОЃЌЙЪAДэЮѓЃЛ
BЃЎШнЦїЕФШнЛ§КЭЛьКЯЦјЬхзмжЪСПЖМВЛБфЃЌЫљвдЛьКЯЦјЬхЕФУмЖШВЛЫцЪБМфИФБфЃЌВЛФмзїЮЊЗДгІДяЕНЦНКтзДЬЌЕФБъжОЃЌЙЪBДэЮѓЃЛ
CЃЎе§ЗДгІЮЊЗХШШЗДгІЃЌЬхЯЕДяЕНЦНКтКѓЃЌЩ§ИпЮТЖШЃЌЦНКтЯђФцЗДгІЗНЯђвЦЖЏЃЌЦјЬхЗжзгЪ§МѕаЁЃЌИљОнM=![]() ЃЌЬхЯЕжаЕФЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПдіДѓЃЌЙЪCе§ШЗЃЛ
ЃЌЬхЯЕжаЕФЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПдіДѓЃЌЙЪCе§ШЗЃЛ
DЃЎКуЮТКубЙЪБЃЌГфШыCH4ЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЃЌЕЊбѕЛЏЮяЕФзЊЛЏТЪдіДѓЃЌЙЪDе§ШЗЁЃ
ЙЪД№АИЮЊЃКCDЃЛ
Ђкt2ЪБШнЛ§РЉДѓЕНдРДЕФ2БЖЃЌзщЗжХЈЖШМѕаЁЃЌИљОнРеЯФЬиСадРэЃЌЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЃЌvе§(N2)МѕаЁЃЌt3ЪБДяЕНЦНКтЃЌМДЭМЯёЪЧЃК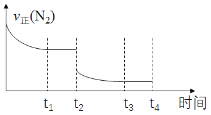 ЁЃ
ЁЃ
ЙЪД№АИЮЊЃК ЁЃ
ЁЃ
(2) ЗДгІIЃК2NO(g)![]() N2(g)ЃЋO2(g) K1=1ЁС1030
N2(g)ЃЋO2(g) K1=1ЁС1030
ЗДгІIIЃК2CO2 (g)![]() 2CO(g)ЃЋO2(g) K2=4ЁС10Ѓ92
2CO(g)ЃЋO2(g) K2=4ЁС10Ѓ92
ОнИЧЫЙЖЈТЩЂй-ЂкЕУ2NO(g)+2CO(g)![]() N2(g) +2CO2(g)ЕФK= K1/K2ЃН2.5ЁС10121ЃЌKжЕдНДѓЃЌЗДгІНјааЕФдНЭъШЋЃЌДгРэТлЩЯРДЫЕЃЌCOгыNOФмЗДгІЭъШЋЃЌ
N2(g) +2CO2(g)ЕФK= K1/K2ЃН2.5ЁС10121ЃЌKжЕдНДѓЃЌЗДгІНјааЕФдНЭъШЋЃЌДгРэТлЩЯРДЫЕЃЌCOгыNOФмЗДгІЭъШЋЃЌ
вђДЫЃЌБОЬте§ШЗД№АИЪЧЃКФмЃЌгЩЗДгІIКЭIIЕФЦНКтГЃЪ§ЃЌПЩжЊ2NO(g)+2CO(g)![]() N2(g) +2CO2(g)ЕФK= K1/K2ЃН2.5ЁС10121ЃЌИУЗДгІЯђе§ЗНЯђЕФЧїЪЦКмДѓЃЌЪЙгУКЯЪЪЕФДпЛЏМСМгПьЗДгІЫйТЪЃЌЛљБОЩЯПЩвдГ§ШЅЮлШОЦјЬхЃЛ
N2(g) +2CO2(g)ЕФK= K1/K2ЃН2.5ЁС10121ЃЌИУЗДгІЯђе§ЗНЯђЕФЧїЪЦКмДѓЃЌЪЙгУКЯЪЪЕФДпЛЏМСМгПьЗДгІЫйТЪЃЌЛљБОЩЯПЩвдГ§ШЅЮлШОЦјЬхЃЛ
ЃЈ3ЃЉNO(g) +NO2(g)+2NH3(g)![]() 2N2(g) + 3H2O(g)ЁЃ
2N2(g) + 3H2O(g)ЁЃ
вбжЊЦНКтЪБЃЌn(NO)=a molЃЌn(NO2)=2a molЃЌn(NH3)=2a molЃЌn(N2)=2b molЃЌ
ЮяжЪБфЛЏЕФЮяжЪЕФСПжЎБШЕШгкЛЏбЇМЦСПЪ§жЎБШЃЌдђn(H2O)=3b molЃЌ
ИљОнN2(g)ЕФЬхЛ§ЗжЪ§ЮЊ1/3ЃЌдђгаЃК![]() =
=![]() ЃЌНтЕУЃЌb=5aЃЌ
ЃЌНтЕУЃЌb=5aЃЌ
ЦНКтЪБNOЁЂNO2ЁЂNH3ЁЂN2ЁЂH2OЕФЮяжЪЕФСПЗжЪ§ЗжБ№ЮЊЃК![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ![]() ЃЌ
ЃЌ
ДЫЪБЕФЦНКтГЃЪ§Kp=![]() =
=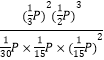 =
=![]() PЁЃ
PЁЃ
вђДЫЃЌБОЬте§ШЗД№АИЪЧЃК![]() PЃЛ
PЃЛ
ЃЈ4ЃЉЕчМЋIЮЊвѕМЋЃЌвѕМЋЩЯЪЧHSO3ЃЛёЕУЕчзгЩњГЩS2O42ЃЃЌдкЫсадЬѕМўЯТЛЙЩњГЩЫЎЃЌЕчМЋЗДгІЮЊЃК2HSO3Ѓ + 2eЃ+ 2H+ = S2O42Ѓ+2H2OЃЌ
вђДЫЃЌБОЬте§ШЗД№АИЪЧЃК2HSO3Ѓ + 2eЃ+ 2H+ = S2O42Ѓ+2H2OЁЃ


 ИпжаБиЫЂЬтЯЕСаД№АИ
ИпжаБиЫЂЬтЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЌЕМВФСЯЮЊОпгаСуЕчзшМАДХадЕФЮяжЪЃЌвдY2O3ЁЂBaCO3КЭCuOЮЊдСЯЃЌОбаФЅЩеНсПЩКЯГЩвЛжжИпЮТГЌЕМЮяжЪYBa2Cu3OxЁЃЯжгћКЯГЩ0.5 molДЫИпЮТГЌЕМЮяЃЌвРЛЏбЇМЦСПЪ§БШР§ашШЁY2O3ЁЂBaCO3КЭCuOЕФЮяжЪЕФСПЗжБ№ЮЊЃЈ ЃЉ
A. 0.50 molЁЂ0.50 molЁЂ0.50 mol B. 0.25 molЁЂ1.0 molЁЂ1.5 mol
C. 0.50 molЁЂ1.0 molЁЂ1.5 mol D. 1.0 molЁЂ0.25 molЁЂ0.17 mol
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖЬжмЦкжїзхдЊЫиAЁЂBЁЂCЁЂDЁЂEЁЂFЕФдзгађЪ§вРДЮдіДѓЃЌдзгКЫЭтЕчзгВуЪ§жЎКЭЮЊ13ЁЃBЕФЛЏКЯЮяжжРрЗБЖрЃЌЪ§ФПХгДѓЃЛCЁЂDЪЧПеЦјжаКЌСПзюЖрЕФСНжждЊЫиЃЌDЁЂEСНжждЊЫиЕФЕЅжЪЗДгІПЩвдЩњГЩСНжжВЛЭЌЕФРызгЛЏКЯЮяЃЛFЮЊЭЌжмЦкдзгАыОЖзюаЁЕФдЊЫиЁЃЪдЛиД№вдЯТЮЪЬтЃК
ЃЈ1ЃЉаДГіAгыDвд1ЁУ1ЕФдзгИіЪ§БШаЮГЩЕФЛЏКЯЮяЕФЕчзгЪНЃК______________ЁЃFЕФРызгНсЙЙЪОвтЭМЮЊ_______________________ЁЃ
ЃЈ2ЃЉBЁЂDаЮГЩЕФЛЏКЯЮяBD2жаДцдкЕФЛЏбЇМќЮЊ________Мќ(ЬюЁАРызгЁБЛђЁАЙВМлЁБЃЌЯТЭЌ)ЁЃAЁЂDЁЂEШ§жждЊЫиаЮГЩЕФЛЏКЯЮяЮЊ____________ЛЏКЯЮяЁЃ
ЃЈ3ЃЉЛЏКЯЮяМзЁЂввгЩAЁЂBЁЂDЁЂEжаЕФШ§жжЛђЫФжжзщГЩЃЌЧвМзЁЂввЕФЫЎШмвКОљГЪМюадЁЃдђМзЁЂввЗДгІЕФРызгЗНГЬЪНЮЊ________________________________ЁЃ
ЃЈ4ЃЉЛЏКЯЮяC2A4КЭC2D4ЕФвКЬхдјБЛгУзїЛ№М§ЭЦНјМСЃЌШМЩеЗДгІЕФЩњГЩЮяЪЧвЛжжЦјЬЌЕЅжЪКЭвЛжжЛЏКЯЮяЃЌЫќУЧЖдЛЗОГЮоЮлШОЁЃ1 mol C2A4вКЬхКЭзуСПC2D4вКЬхЭъШЋЗДгІЩњГЩСНжжЦјЬхЪБЗХГіШШСП516.8 kJЃЌдђИУЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊ_________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПэкЃЈTeЃЉЙуЗКгУгкВЪЩЋВЃСЇКЭЬеДЩЁЃЙЄвЕЩЯгУОЋСЖЭЕФбєМЋФрЃЈКЌгажЪСПЗжЪ§ЮЊ8%ЕФTeO2ЁЂЩйСПAgЁЂAu)ЮЊдСЯжЦБИЕЅжЪэкЕФвЛжжЙЄвеСїГЬШчЯТЃЌЃЈвбжЊTeO2ЮЂШмгкЫЎЃЌвзШмгкЧПЫсКЭЧПМюЃЉЃЌЯТСагаЙиЫЕЗЈВЛе§ШЗЕФЪЧ
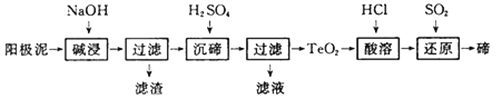
A. НЋбєМЋФрбаФЅЁЂЗДгІЪЪЕБМгШШЖМгаРћгкЬсИпЁАМюНўЁБЕФЫйТЪКЭаЇТЪ
B. ЁАМюНўЁБЪБЗЂЩњжївЊЗДгІЕФРызгЗНГЬЪНЮЊTeO2+2OHЃЃНTeO32Ѓ+H2O
C. ЁАГСэкЁБЪБЮЊЪЙэкдЊЫиГСЕэГфЗжЃЌгІМгШыЙ§СПЕФСђЫс
D. ШєЬсШЁЙ§ГЬэкдЊЫиЕФЛиЪеТЪЮЊ90%ЃЌдђДІРэ1kgетжжбєМЋФрзюЩйашЭЈШыБъзМзДПіЯТSO2 20.16L
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкКЌЕЊЛЏКЯЮяЕФаджЪа№Ъіе§ШЗЕФЪЧ(ЁЁЁЁ)
A.ПЩгУЬњжЦШнЦїДЂДцЯЁЯѕЫс
B.ЪЕбщЪвгУХХПеЦјМЏЦјЗЈЪеМЏNOЦјЬх
C.ЪЕбщЪвПЩгУАБЫЎгыСђЫсТСШмвКЗДгІжЦШЁЧтбѕЛЏТС
D.NO2гыЫЎЗЂЩњЛЏКЯЗДгІЩњГЩЯѕЫс
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМЫљЪОЃЌзЖаЮЦПФкЪЂгаЦјЬхXЃЌЕЮЙмФкЪЂгавКЬхYЃЎШєМЗбЙЕЮЙмНКЭЗЃЌЪЙвКЬхYЕЮШыЦПжаЃЌеёЕДЃЌЙ§вЛЛсПЩМћаЁЦјЧђaЙФЦ№ЃЎЦјЬхXКЭвКЬхYВЛПЩФмЪЧЃЈ ЃЉ

AЃЎXЪЧNH3ЃЌYЪЧЫЎ
BЃЎXЪЧSO2ЃЌYЪЧNaOHХЈШмвК
CЃЎXЪЧCO2ЃЌYЪЧЯЁСђЫс
DЃЎXЪЧHClЃЌYЪЧNaNO3ЯЁШмвК
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгаЛњЮяYЃЈ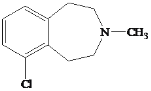 ЃЉЪЧвЛжжжЮСЦаФбЊЙмКЭИпбЊбЙЕФвЉЮяЃЌФГбаОПаЁзщвдМзБНЁЂввЯЉЕШЮяжЪЮЊжївЊдСЯЃЌЭЈЙ§вдЯТТЗЯпКЯГЩЃК
ЃЉЪЧвЛжжжЮСЦаФбЊЙмКЭИпбЊбЙЕФвЉЮяЃЌФГбаОПаЁзщвдМзБНЁЂввЯЉЕШЮяжЪЮЊжївЊдСЯЃЌЭЈЙ§вдЯТТЗЯпКЯГЩЃК
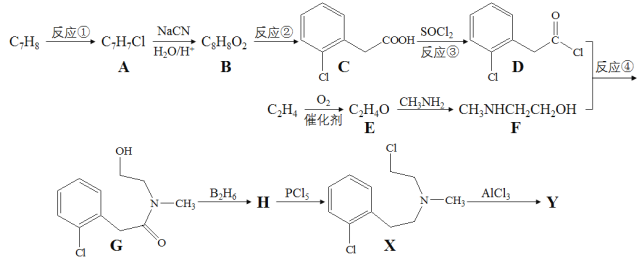
вбжЊЃКRX+NaCN![]() RCN
RCN![]() RCOOH
RCOOH
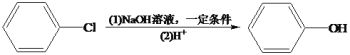
ЧыЛиД№ЃК
ЃЈ1ЃЉаДГіЛЏКЯЮяHЕФНсЙЙМђЪН_______________ЁЃ
ЃЈ2ЃЉЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ______________ЁЃ
AЃЎЗДгІЂйЕФЪдМСгыЬѕМўЮЊCl2/Йтее
BЃЎЛЏКЯЮяEФмЗЂЩњвјОЕЗДгІ
CЃЎЛЏКЯЮяGЁњYЕФзЊЛЏЙ§ГЬжаЃЌЩцМАЕФЗДгІРраЭгаШЁДњЗДгІЁЂМгГЩЗДгІ
DЃЎYЕФЗжзгЪНЮЊC11H13NCl
ЃЈ3ЃЉаДГіЗДгІЂмЕФЛЏбЇЗНГЬЪН________________ЁЃ
ЃЈ4ЃЉЗМЯузхЛЏКЯЮяMЪЧBЕФЭЌЗжвьЙЙЬхЃЌMКЌгаЖўИіСљдЊЛЗЃЌдђMПЩФмЕФНсЙЙга_______________ЁЃ
ЃЈ5ЃЉвбжЊвЛИіЬМдзгЩЯСЌгаСНИієЧЛљЪЧВЛЮШЖЈЕФЃЌЛсЭбЫЎзЊЛЏЮЊєЪЛљЁЃЪдаДГігЩCЕФвЛжжЭЌЗжвьЙЙЬхжЦБИКЯГЩ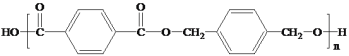 ЕФЯпТЗЭМЁЃ___________
ЕФЯпТЗЭМЁЃ___________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПРћгУЯТЭМЫљЪОзАжУвЛЖЈЬѕМўЯТПЩЪЕЯжгаЛњЮяЕФЕчЛЏбЇДЂЧт(КіТдЦфЫћгаЛњЮя)ЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
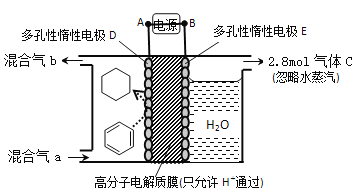
A. AЮЊЕчдДЕФИКМЋ
B. EМЋЕФЕчМЋЪНЮЊ2H2O-4e-=4H++O2Ёќ
C. DМЋЩњГЩФПБъВњЮяЕФЕчМЋЪНЮЊC6H6+6H++6e-=C6H12
D. ИУзАжУЕФЕчСїаЇТЪ![]() 75ЃЅ
75ЃЅ![]() ЃЌдђbжаЛЗМКЭщдіМг2.8mol
ЃЌдђbжаЛЗМКЭщдіМг2.8mol
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛЖЈЮТЖШЯТЃЌКуШнУмБеШнЦїжаЗЂЩњЗДгІЃК4NH3ЃЈgЃЉ+5O2ЃЈgЃЉ![]() 4NOЃЈgЃЉ+6H2OЃЉЃЈgЃЉЃЌЯТСаа№ЪіВЛФмЫЕУїИУЗДгІДяЦНКтЕФЪЧЃЈЁЁЁЁЃЉ
4NOЃЈgЃЉ+6H2OЃЉЃЈgЃЉЃЌЯТСаа№ЪіВЛФмЫЕУїИУЗДгІДяЦНКтЕФЪЧЃЈЁЁЁЁЃЉ
A.VЃЈе§ЃЉЃЈO2ЃЉЃН![]() VЃЈФцЃЉЃЈNOЃЉB.УмБеШнЦїФкЦјЬхЕФУмЖШВЛдйИФБф
VЃЈФцЃЉЃЈNOЃЉB.УмБеШнЦїФкЦјЬхЕФУмЖШВЛдйИФБф
C.УмБеШнЦїЕФбЙЧПВЛБфD.ЕЊЦјЕФХЈЖШВЛдйИФБф
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com