
【题目】菠萝酯(F)是一种具有菠萝香味的赋香剂,其合成路线如下:
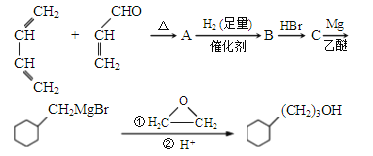


(1)A的结构简式为________,A中所含官能团的名称是_____。
(2)A→B反应类型是________; B→C反应,除HBr之外还需要的试剂和条件是________。
(3)E的某种同分异构体的一氯代物只有一种,该同分异构体的结构简式为________。
(4)1mol菠萝酯(F)与氢气反应,最多消耗氢气____mol。
(5)结合题干信息,以乙烯和环氧乙烷(![]() )为原料制备1丁醇,设计合成路线________(其它试剂任选)。
)为原料制备1丁醇,设计合成路线________(其它试剂任选)。
(合成路线常用表示方法为:A ![]() B ……
B ……![]() 目标产物)
目标产物)
【答案】 ![]() 醛基、碳碳双键 加成或还原 浓硫酸、加热
醛基、碳碳双键 加成或还原 浓硫酸、加热 ![]() (或CH3COCH3) 1
(或CH3COCH3) 1 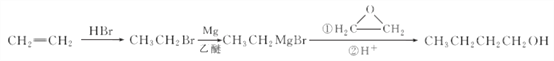
【解析】根据题目所给信息,可知1,3-丁二烯与丙烯醛发生加成反应反应生成A为![]() ,A与足量的氢气发生加成反应生成B为
,A与足量的氢气发生加成反应生成B为![]() ,B在HBr条件下发生取代反应生成C为
,B在HBr条件下发生取代反应生成C为![]() ,C与Mg在干醚的条件下得到
,C与Mg在干醚的条件下得到![]() ,
,![]() 发生信息中反应得到
发生信息中反应得到![]() ,再发生催化氧化反应生成
,再发生催化氧化反应生成![]() ,
,![]() 被酸性高锰酸钾溶液溶液氧化生成D为
被酸性高锰酸钾溶液溶液氧化生成D为![]() ,对比D与F的结构可知,D与CH2=CHCH2OH反应酯化反应得到F,故E为CH2=CHCH2OH。
,对比D与F的结构可知,D与CH2=CHCH2OH反应酯化反应得到F,故E为CH2=CHCH2OH。
(1)由上述分析可知,A的结构简式为![]() ,所含官能团有:醛基、碳碳双键,故答案为:
,所含官能团有:醛基、碳碳双键,故答案为:![]() ;醛基、碳碳双键;
;醛基、碳碳双键;
(2)由A生成B的反应类型属于加成反应,B在HBr条件下发生取代反应生成C为![]() ,B→C反应,除HBr之外还需要的试剂和条件是浓硫酸、加热,故答案为:加成或还原;浓硫酸、加热;
,B→C反应,除HBr之外还需要的试剂和条件是浓硫酸、加热,故答案为:加成或还原;浓硫酸、加热;
(3)E为CH2=CHCH2OH,E的某同分异构体只有一种相同化学环境的氢,该同分异构体的结构简式为:![]() ,故答案为:
,故答案为:![]() ;
;
(4)菠萝酯(F)中只有碳碳双键能够与氢气发生加成反应,1mol菠萝酯(F)与氢气反应,最多消耗氢气1mol,故答案为:1;
(5)由转化关系中反应可知,乙烯与溴化氢加成生成溴乙烷,溴乙烷与Mg在干醚的条件下得到CH3CH2MgBr,再与环氧乙烷在酸性条件下得到1-丁醇,合成路线流程图为: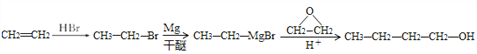 ,故答案为:
,故答案为: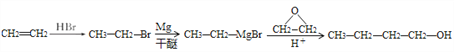 。
。


科目:高中化学 来源: 题型:
【题目】胶体区别于其他分散系的本质特征是( )
A. 胶体能产生丁达尔现象 B. 胶体是纯净物,其他分散系是混合物
C. 胶体的分散质能透过滤纸 D. 胶体的分散质粒子直径在1~100nm之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中,金属元素大多以化合态存在,通过金属冶炼得到金属单质。
工业上生产Na、Ca、Mg都用电解其熔融的氯化物,但生产钾是用金属钠和熔化的KCl在一定的条件下反应制取:
KCl + Na![]() NaCl + K + Q (Q<0)
NaCl + K + Q (Q<0)
有关数据如下表:
熔点℃ | 沸点℃ | 密度 (g/cm3) | |
Na | 97.8 | 882.9 | 0.97 |
K | 63.7 | 774 | 0.86 |
NaCl | 801 | 1413 | 2.165 |
KCl | 770 | 1500 | 1.984 |
(1)请结合平衡移动理论分析,为什么能用该反应制备金属钾。
_______________________________________。
(2)在常压下金属钾转为气态从反应混合物中分离的最低温度约为_____℃,而反应的最高温度应低于_____℃。
(3)在制取金属钾的过程中,为了提高原料的转化率可采取的措施有__________。(任写两点)
(4)相比于电解熔融氯化钾,此方法的优点有_____________________。
(5)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为![]() ________。
________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为____________,被选作相对原子质量标准的核素是 ______(填核素符号)
(2)由A、B、W三种元素组成的18电子微粒的电子式为___________________
(3)A、B、W、D、E五种元素的原子半径由小到大的顺序为__________ ( 填元素符号)
(4)元素D的单质在一定条件下,能与A单质化合生成DA,DA能与水反应放氢气,若将1molDA和1molE单质混合加入足量的水,充分反应后成气体的体积是___________________(标准状况下)
(5)若要比较D比E的金属性强弱,下列实验方法可行的是 (____________)
A.将单质D置于E的盐溶液中,若D不能置换出单质E,说明D的金属性弱
B.比较D和E的最高价氧化物对应水化物的水溶性,前者比后者溶解度大,故前者金属性强
C.将D、E的单质分别投入到同浓度的盐酸中,观察到D反应更剧烈,说明D的金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的结构简式为 ,下列有关A的说法中正确的是( )
,下列有关A的说法中正确的是( )
A. 常温下,1molA能消耗2molNaOH
B. 1molA与足量的金属钠反应能生成22.4L氢气
C. 1 molA完全燃烧能消耗6molO2
D. A在一定条件下发生酯化反应能生成六元环酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高倩同学在做实验时引发了镁失火,她立即拿起二氧化碳灭火器欲把火扑灭,却被实验老师及时制止。原因是CO2可以支持镁燃烧发生以下反应:2Mg+CO2![]() 2MgO+C,下列关于该反应的判断正确的是( )
2MgO+C,下列关于该反应的判断正确的是( )
A. Mg元素化合价由0价升高到+2价,所以MgO是还原产物
B. 由此反应可以判断氧化性CO2>MgO,还原性Mg>C
C. CO2作氧化剂,表现氧化性,发生氧化反应
D. Mg原子失去的电子数目等于氧原子得到的电子数目
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法中正确的是
A.1mol/L盐酸溶液中含H+ 1 mol
B.常温常压下,1mol CH4的质量为16g/mol
C.28g C2H4和C3H6混合气体原子数目为6NA
D.标准状况下,2.24 L H2O中所含原子数均为0.3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com