
【题目】根据能量变化示意图,下列热化学方程式正确的是( )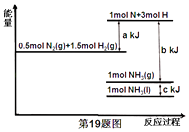
A.N2(g)+3H2(g)=2NH3(g)△H=﹣(b﹣a)kJmol﹣1
B.N2(g)+3H2(g)=2NH3(g)△H=﹣(a﹣b)kJmol﹣1
C.2NH3(l)=N2(g)+3H2(g)△H=2(a+b﹣c)kJmol﹣1
D.2NH3(l)=N2(g)+3H2(g)△H=2(b+c﹣a)kJmol﹣1
【答案】D
【解析】由图可知, ![]() N2(g)+
N2(g)+ ![]() H2(g)=NH3(g)△H=(a﹣b)kJmol﹣1,
H2(g)=NH3(g)△H=(a﹣b)kJmol﹣1, ![]() N2(g)+
N2(g)+ ![]() H2(g)=NH3(l)△H=(a﹣b﹣c)kJmol﹣1,则
H2(g)=NH3(l)△H=(a﹣b﹣c)kJmol﹣1,则
A.N2(g)+3H2(g)=2NH3(g)△H=﹣2(b﹣a)kJmol﹣1,故A错误;
B.N2(g)+3H2(g)=2NH3(g)△H═﹣2(b﹣a)kJmol﹣1,故B错误;
C.物质的量与热量成正比、互为可逆反应的焓变的数值相同而符号相反,则2NH3(l)=N2(g)+3H2(g)△H=2(﹣a+b+c)kJmol﹣1,故C错误;
D.结合选项C可知,2NH3(l)=N2(g)+3H2(g)△H=2(b+c﹣a)kJmol﹣1,故D正确;
所以答案是:D.
【考点精析】通过灵活运用反应热和焓变,掌握在化学反应中放出或吸收的热量,通常叫反应热即可以解答此题.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. ![]() 结论:CH4的燃烧热为801.3 kJ/mol
结论:CH4的燃烧热为801.3 kJ/mol
B. ![]() (灰锡为粉末状)结论:锡制品在寒冷的冬天因易转化为灰锡而损坏
(灰锡为粉末状)结论:锡制品在寒冷的冬天因易转化为灰锡而损坏
C. 稀溶液中有![]() 结论:将盐酸与氨水的稀溶液混合后,若生成1mol H20,则会放出57.3kJ的能量
结论:将盐酸与氨水的稀溶液混合后,若生成1mol H20,则会放出57.3kJ的能量
D. ![]() AH=一393.5 kJ/mol,
AH=一393.5 kJ/mol,![]() 结论:相同条件下金刚石性质比石墨稳定
结论:相同条件下金刚石性质比石墨稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的工作原理及电池中发生的主要反应如图所示。下列说法错误的是
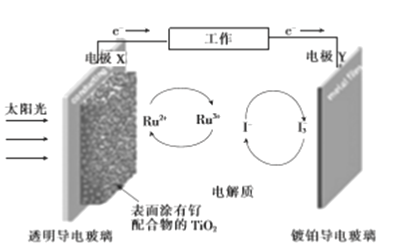
A. 电池工作时,光能转变为电能,X为电池的负极
B. 镀铂导电玻璃上发生氧化反应生成I-
C. 电解质溶液中发生反应:2Ru3++3I-![]() 2Ru2++I3-
2Ru2++I3-
D. 电池工作时,电解质溶液中I-和I3-的浓度基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)常温下,0.1mol/L 的CH3COOH溶液中有1%的CH3COOH分子发生电离,则溶液的pH=;可以使0.10 mol·L-1 CH3COOH的电离程度增大的是
a.加入少量0.10 mol·L-1的稀盐酸
b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1
d.加入少量冰醋酸
e.加入少量氯化钠固体
f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)V(醋酸)(填“>”、“<”或“=”)。
(3)0.1mol/L的某酸H2A的pH=4,则H2A的电离方程式为。
(4)25℃时,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,若所得混合溶液的pH=6,则NaOH溶液与盐酸溶液的体积比为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用二氧化锰和足量的浓盐酸反应中制备氯气,如果有34.8 g二氧化锰被还原,那么被氧化的HC1的物质的量是多少?得到的氯气的物质的量是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米材料一直是人们研究的重要课题,例如纳米级Fe粉表面积大,具有超强的磁性,高效催化性等优良的性质。
I、实验室采用气相还原法制备纳米级Fe,其流程如图所示:

(1)纳米级Fe和稀盐酸反应的离子方程式为_______________________________。
(2)如何将FeCl2·nH2O固体加热脱水制得无水FeCl2 _____________________________________(用简要文字描述)。
(3)生成纳米级Fe的化学方程式为______________________________________。
II、查阅资料:在不同温度下,纳米级Fe粉与水蒸气反应的固体产物不同,温度低于570℃时生成FeO,高于570℃时生成Fe3O4。甲同学用如图甲装置所示进行纳米级Fe粉与水蒸气反应的实验,乙同学用图乙所示的装置进行纳米级Fe粉与水蒸气的反应并验证产物。
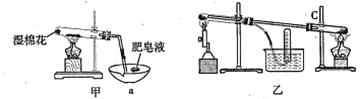
(4)甲装置中纳米级Fe粉与水蒸气反应的化学方程式是 ______________________。
(5)甲装置中仪器a的名称为_______________________。
(6)乙同学为探究实验结束后试管内的固体物质成分,进行了下列实验:
实验步骤 | 实验操作 | 实验现象 |
I | 将反应后得到的黑色粉末X(假定为均匀的),取出少量放入另一试管中,加入少量盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
II | 向实验I得到的溶液中滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
根据以上实验,乙同学认为该条件下反应的固体产物为FeO。
丙同学认为乙同学的结论不正确,他的理由是______(用简要文字描述)。
(7)丁同学称取5.60gFe粉,用乙装反应一段时间后,停止加热。将试管内的固体物质在干燥器中冷却后,称得质量为6.88g,则丁同学实验后的固体物质中氧化物的质量分数为________(结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语对事实的表述不正确的是( )
A. 氢氧化钠溶液与二氧化硅反应:SiO2+2OH-=SiO32-+H2O
B. 常温时,0.1mol·L-1氨水的pH=11.1:NH3·H2O![]() NH4++OH-
NH4++OH-
C. 由Na和Cl形成离子键的过程: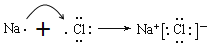
D. 大理石与醋酸反应CO32-+2CH3COOH=2CH3COO-+H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10 molL-1 NaOH溶液滴定20.00mL 0.10molL-1的CH3COOH溶液,所得滴定曲线如图。下列说法正确的是
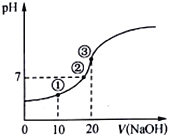
A. 点①所示溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B. 点②所示溶液中:c(Na+)=c(CH3COO-),酸碱恰好完全反应
C. 点③所示溶液中:c(OH-)-(H+)=c(CH3COOH)
D. 滴定过程中:c(CH3COO-)+c(CH3COOH)= 0.10molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质和应用对应关系正确的是
A. 晶体硅熔点高、硬度大,是制造太阳能电池和计算机芯片的主要材料
B. 氧化铝熔点高,常用于耐高温材料
C. 明矾溶于水能形成胶体,可用于自来水的杀菌消毒
D. 苏打溶液呈弱碱性,可用作胃酸中和剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com